题目内容
下列说法中,正确的是( )
| A、将NO2通入FeSO4溶液中不会有明显现象 |
| B、2L 0.5mol/L的盐酸和1L 0.5mol/L的硫酸PH相等 |
| C、饱和氯水中:c(H+)>c(Cl-)>c(HClO)>c(ClO-) |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下反应的△H不相同 |
考点:氮的氧化物的性质及其对环境的影响,pH的简单计算,离子浓度大小的比较,氯气的化学性质
专题:元素及其化合物
分析:A.二氧化氮与水反应生成硝酸和一氧化氮,硝酸能够将亚铁离子氧化成铁离子,溶液由浅绿色变成棕黄色;
B.酸溶液的pH取决于溶液中氢离子浓度,该盐酸溶液中氢离子浓度为0.5mol/L,硫酸溶液中氢离子浓度为1mol/L;
C.饱和氯水中,部分氯气与水反应生成等物质的量的强电解质氯化氢和弱电解质次氯酸,据此判断溶液中各离子浓度关系;
D.根据盖斯定律可知,反应中的能量变化与反应物、生成物有关,与反应途径无关.
B.酸溶液的pH取决于溶液中氢离子浓度,该盐酸溶液中氢离子浓度为0.5mol/L,硫酸溶液中氢离子浓度为1mol/L;
C.饱和氯水中,部分氯气与水反应生成等物质的量的强电解质氯化氢和弱电解质次氯酸,据此判断溶液中各离子浓度关系;
D.根据盖斯定律可知,反应中的能量变化与反应物、生成物有关,与反应途径无关.
解答:
解:A.将NO2通入FeSO4溶液中,二氧化氮与水反应生成硝酸,硝酸将亚铁离子氧化成铁离子,溶液颜色由浅绿色变成了棕黄色,具有明显的现象,故A错误;
B.2L0.5mol/L的盐酸中氢离子浓度为0.5mol/L,1L 0.5mol/L的硫酸中氢离子浓度为1mol/L,两溶液中氢离子浓度不同,溶液的pH不相等,故B错误;
C.饱和氯水中,氯气与水发生反应:Cl2+H2O?HCl+HClO,部分氯气转化成等物质的量的氯化氢和次氯酸,HCl为强电解质,HClO为弱电解质,所以溶液中离子浓度关系为:c(H+)>c(Cl-)>c(HClO)>c(ClO-),故C正确;
D.根据盖斯定律可知,同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下反应的△H一定相同,故D错误;
关系C.
B.2L0.5mol/L的盐酸中氢离子浓度为0.5mol/L,1L 0.5mol/L的硫酸中氢离子浓度为1mol/L,两溶液中氢离子浓度不同,溶液的pH不相等,故B错误;
C.饱和氯水中,氯气与水发生反应:Cl2+H2O?HCl+HClO,部分氯气转化成等物质的量的氯化氢和次氯酸,HCl为强电解质,HClO为弱电解质,所以溶液中离子浓度关系为:c(H+)>c(Cl-)>c(HClO)>c(ClO-),故C正确;
D.根据盖斯定律可知,同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下反应的△H一定相同,故D错误;
关系C.
点评:本题考查了二氧化氮的化学性质、氯气的化学性质、离子浓度大小比较、溶液pH的简单计算等知识,题目难度中等,注意掌握常见元素单质及其化合物的性质,明确溶液酸碱性与溶液pH的关系,试题有利于培养学生的分析、理解能力及灵活应用所学知识解决简单化学问题的能力.

练习册系列答案
相关题目
 室温下,在0.2mol?L-1 Al2(SO4)3溶液中,逐滴加入1.0mol?L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是( )
室温下,在0.2mol?L-1 Al2(SO4)3溶液中,逐滴加入1.0mol?L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是( )| A、a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH-?Al(OH)3 |
| B、a-b段,溶液pH增大,Al3+浓度不变 |
| C、b-c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D、d点时,Al(OH)3沉淀开始溶解 |
下列说法正确的是( )
| A、煤的干馏、石油的分馏都是物理变化 |
| B、工业上常用澄清石灰水和氯气反应制漂白粉 |
| C、蛋白质溶液中加入硫酸铵溶液和硫酸铜溶液均能产生白色沉淀,都属于“盐析” |
| D、二氧化硅可以用于制造光导纤维,光导纤维遇强碱会“断路” |
某溶液可能含有Cl-、SO42-、CO32-、OH-、NH4+、Al3+、Fe3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g固体;向上述滤液中加足量BaCl2溶液,得到 6.99g不溶于盐酸的沉淀.下列关于原溶液的说法正确的是( )
| A、原溶液中至少存在3种离子 |
| B、原溶液中一定不存在的离子是:Cl-、CO32-、OH- |
| C、原溶液中可能存在的离子有:Cl-、Al3+和K+ |
| D、原溶液中一定存在的离子是:NH4+、Fe3+、SO42-和Cl-,且c(Cl-)≥0.2mol/L |
有关烷烃的叙述:①都是易燃物②特征反应是取代反应③碳原子数相邻的两个烷烃分子在组成上相差一个“-CH3”,其中正确的是( )
| A、①② | B、①③ | C、① | D、②③ |
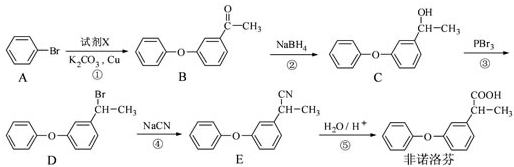
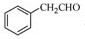 为原料制备
为原料制备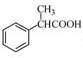 的合成路线流程图(无机试剂任用),合成路线路程图示例如下:
的合成路线流程图(无机试剂任用),合成路线路程图示例如下: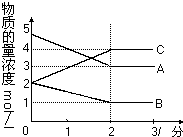 在密闭容器中,某反应在不同反应时间各物质的量的变化情况如右图所示(各物质均为气体).
在密闭容器中,某反应在不同反应时间各物质的量的变化情况如右图所示(各物质均为气体).