题目内容
2.下列性质的比较中,不正确的是( )| A. | 稳定性:Na2CO3>NaHCO3 | B. | 熔点:生铁>纯铁 | ||
| C. | 酸性:H2CO3>HClO | D. | 氧化性:Fe3+>Cu2+ |
分析 A.碳酸钠加热不易分解;
B.生铁是合金,合金的熔点一般小于各组分的熔点;
C.次氯酸为弱酸,酸性比碳酸还弱;
D.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性.
解答 解:A.因2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,而碳酸钠加热不分解,故A正确;
B.生铁是合金,熔点小于纯铁的熔点,故熔点为纯铁>生铁,故B错误;
C.次氯酸为弱酸,酸性比碳酸还弱,通过漂白粉的漂白原理可以证明,故C正确;
D.反应2Fe3++Cu=2Fe2++Cu2+中,氧化剂Fe3+的氧化性大于氧化产物Cu2+的氧化性,故D正确,故选B.
点评 本题主要考查的是物质稳定性比较、氧化性强弱判断以及酸性强弱比较等,综合性较强,但是难度不大.

练习册系列答案
相关题目
1.DDT是被禁用的有机污染物,它的结构简式为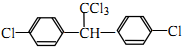 .下列有关DDT的说法正确的是( )
.下列有关DDT的说法正确的是( )
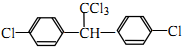 .下列有关DDT的说法正确的是( )
.下列有关DDT的说法正确的是( )| A. | 它属于芳香烃 | B. | 分子中最多有23个原子共平面 | ||
| C. | 分子式为C14H9Cl5 | D. | 能发生水解反应和消去反应 |
10.室温下,将0.1molK2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质.有关结论正确的是( )
| 加入的物质 | 结论 | |
| A | 100mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
| B | 0.01molK2O | 溶液中$\frac{c(HC{{O}_{3}}^{-})}{c(O{H}^{-})}$ 增大 |
| C | 50mL 1mol/LH2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| D | 0.1molKHSO4固体 | 反应结束后,溶液pH=7 |
| A. | A | B. | B | C. | C | D. | D |
7.下列除杂质的操作中不正确的是( )
| A. | 除去SO2中的少量HCl:通入饱和NaHSO3溶液的洗气瓶,干燥后收集气体 | |
| B. | FeCl2溶液中混有FeCl3:加入过量铁粉充分反应后过滤 | |
| C. | Na2CO3固体中混有少量NaHCO3:加入适量NaOH溶液 | |
| D. | 除去SiO2中的少量Al2O3:加入适量稀硫酸充分反应后过滤 |
14.关于下列四个图象的说法中正确的是( )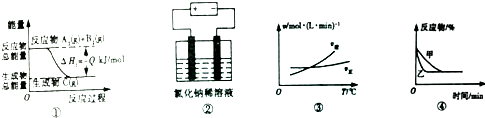

| A. | 图①表示可逆反应A2(g)+B2(g)?C(g)的△H1大于0 | |
| B. | 图②是电解氯化钠稀溶液的电解池,其中阴、阳极产生气体的体积之比一定为1:1 | |
| C. | 图③表示可逆反应A2(g)+3B2(g)?2AB3(g)的△H小于0 | |
| D. | 图④表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙曲线对应的压强大 |
11.下列说法不正确的是( )
| A. | 反应是放热还是吸热必须看生成物和反应物所具有的总能量的相对大小 | |
| B. | 绿色植物进行光合作用时,将太阳能转化为化学能储存起来 | |
| C. | 吸热反应都要加热才能进行 | |
| D. | 物质的化学能可以在一定条件下转化为热能、电能为人类所利用 |
12.在一定温度下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法中,正确的是( )
| A. | n(Na+)+n(H+)=n(HCO3-)+n(CO32-)+n(OH-) | |
| B. | 通入CO2,平衡向正反应方向移动 | |
| C. | 加入少量的NaOH固体,平衡向逆反应方向移动,溶液pH减小 | |
| D. | 稀释溶液,Na2CO3水解程度增大,水解平衡常数增大 |
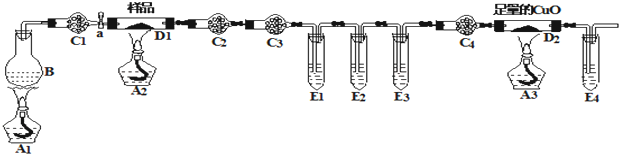
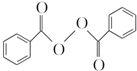 )过去常用作面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程图如图:
)过去常用作面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程图如图: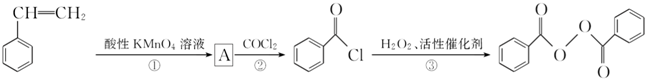
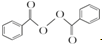 +2H2O→2
+2H2O→2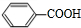 +H2O2;
+H2O2;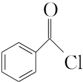 )能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成的有机产物的名称苯甲酸乙酯;
)能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成的有机产物的名称苯甲酸乙酯;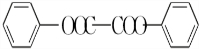 (或
(或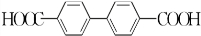 或
或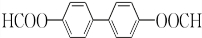 .;
.;