题目内容
把3.0mol/L CuCl2溶液300ml和2.0mol/L FeCl3溶液200mol混合(假设混合后溶液的体积等于混合前两种溶液的体积之和).计算:
(1)混合液中Cu2+、Fe3+、Cl-的物质的量浓度;
(2)向溶液中加入足量铁粉,经足够长的时间后,铁粉有剩余.此溶液中Fe2+的物质的量浓度;
(3)问参加反应的铁粉的质量.
(1)混合液中Cu2+、Fe3+、Cl-的物质的量浓度;
(2)向溶液中加入足量铁粉,经足够长的时间后,铁粉有剩余.此溶液中Fe2+的物质的量浓度;
(3)问参加反应的铁粉的质量.
考点:化学方程式的有关计算,物质的量浓度的相关计算
专题:计算题
分析:(1)根据稀释定律c1V1=c2V2计算;
(2)反应后溶液变为FeCl2溶液,依据Cl守恒解答即可;
(3)依据铁元素守恒解答即可.
(2)反应后溶液变为FeCl2溶液,依据Cl守恒解答即可;
(3)依据铁元素守恒解答即可.
解答:
解:(1)根据稀释定律,c(CuCl2)=c(Cu2+)=
=1.8mol/L,同理c(Fe3+)=
=0.8mol/L,故C(Cl-)=
=6mol/L,故答案为:1.8mol/L,0.8mol/L,6mol/L;
(2)反应后的溶液全部是FeCl2溶液,c(FeCl2)=
c(Cl-)=3.0mol/L,故答案为:3.0 mol/L;
(3)依据(2)得出n(FeCl2)=3.0mol/L×0.5L=1.5mol,原溶液中含有n(Fe3+)=0.4mol,故加入n(Fe)=1.5mol-0.4mol=1.1mol,质量为:1.1mol×56g/mol=61.6g,故答案为:61.6g.
| 3.0mol/L×300mL |
| 300mL+200mL |
| 2.0mol/L×200mL |
| 300mL+200mL |
| 3.0mol/L×300mL×2+2.0mol/L×200mL×3 |
| 300mL+200mL |
(2)反应后的溶液全部是FeCl2溶液,c(FeCl2)=
| 1 |
| 2 |
(3)依据(2)得出n(FeCl2)=3.0mol/L×0.5L=1.5mol,原溶液中含有n(Fe3+)=0.4mol,故加入n(Fe)=1.5mol-0.4mol=1.1mol,质量为:1.1mol×56g/mol=61.6g,故答案为:61.6g.
点评:本题考查物质的量浓度有关计算,难度不大,注意稀释定律的运用,注意对公式的理解与灵活运用,了解电解质浓度与电解质离子浓度关系.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
下列离子方程式书写不正确的是( )
| A、碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O | ||||
| B、含等物质的量的硫酸氢钠与氢氧化钡两溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | ||||
| C、用稀硝酸浸泡做过银镜反应的试管:3Ag+4H++NO3-=3Ag++NO↑+2H2O | ||||
D、用两个铜电极电解饱和食盐水:2Cl-+2H2O
|
 下面给出了四种烃A、B、C、D的相关信息:
下面给出了四种烃A、B、C、D的相关信息: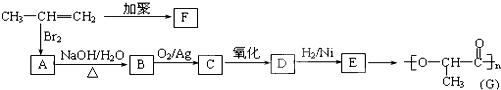
 利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.
利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示. 如图是干冰的晶胞结构示意图.请完成下列问题:
如图是干冰的晶胞结构示意图.请完成下列问题: