题目内容
6.下列有关溶液中粒子浓度的关系式正确的是( )| A. | 25℃,0.1mol/L pH=4.5 的NaHC2O4溶液 c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| B. | 向0.2mol/L的NaHCO3溶液中加入等体积的0.1mol/L的NaOH溶液c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) | |
| C. | 常温下,氯化铵和氨水的混合溶液其pH=7,c(Cl-)=0.1mol/L c(Cl-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 浓度均为0.1mol/L的醋酸钠和醋酸的混合溶液中c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
分析 A.25℃,0.1mol/L的NaHC2O4溶液pH=4.5,说明HC2O4-电离程度大于水解程度,但都较小;
B.向0.2mol/L的NaHCO3溶液中加入等体积的0.1mol/L的NaOH溶液,反应后溶液中溶质为等物质的量浓度的Na2CO3和NaHCO3,任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
C.常温下,氯化铵和氨水的混合溶液其pH=7,溶液呈中性,则c(OH-)=c(H+),根据电荷守恒判断 c(Cl-)、c(NH4+)相对大小;
D.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断.
解答 解:A.25℃,0.1mol/L的NaHC2O4溶液pH=4.5,说明HC2O4-电离程度大于水解程度,所以c(C2O42-)>c(H2C2O4),但电离程度和水解程度都较小,所以存在 c(HC2O4-)>c(C2O42-)>c(H2C2O4),故A正确;
B.向0.2mol/L的NaHCO3溶液中加入等体积的0.1mol/L的NaOH溶液,反应后溶液中溶质为等物质的量浓度的Na2CO3和NaHCO3,任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-),故B错误;
C.常温下,氯化铵和氨水的混合溶液其pH=7,溶液呈中性,则c(OH-)=c(H+),根据电荷守恒得 c(Cl-)=c(NH4+),溶液中c(OH-)=c(H+)且较小,所以离子浓度大小顺序是 c(Cl-)=c(NH4+)>c(OH-)=c(H+),故C错误;
D.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),根据物料守恒2c(Na+)=c(CH3COO-)+c(CH3COOH),所以得c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),即c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)],故D正确;
故选AD.
点评 本题考查离子浓度大小比较,为高频考点,明确溶液中溶质及其性质是解本题关键,注意电荷守恒和物料守恒的灵活运用,题目难度不大.

| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1 000 | 850 | 690 | 625 | 400 |
| A. | 反应I2(aq)+I-(aq)?═?I3-(aq)的△H>0 | |
| B. | 利用该反应可以除去硫粉中少量的碘单质 | |
| C. | 在上述平衡体系中加入苯,平衡不移动 | |
| D. | 25℃时,向溶液中加入少量KI固体,平衡常数K小于690 |
| A. | AlON和石英的化学键类型相同 | B. | 电解熔融AlON可得到Al | ||
| C. | AlON的N元素化合价为-1 | D. | AlON和石英晶体类型相同 |
| A. | 氯水 | B. | 氢硫酸 | C. | 烧碱 | D. | 绿矾 |
 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:(1)钠铝合金可作核反应堆的载热介质.取1.46g的钠铝合金放入水中,合金全部溶解,放出1.12L氢气(标准状况),则该钠铝合金的化学式为Na2Al.
(2)NaCN是一种剧毒的化工原料,可用双氧水处理含NaCN的废液,发生反应的方程式为:NaCN+H2O2+H2O=NaHCO3+NH3.若处理含NaCN 4.90g的废液,需用15%的H2O221.65mL.(已知15% H2O2的密度是1.047g/mL)(保留2位小数)
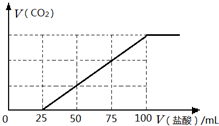
(3)向100mL NaOH溶液中通入一定量的CO2气体,充分反应后得到溶液A,再向A中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.试计算溶液A的溶质成份及其物质的量.
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
| A. | 氯化钠 | B. | 盐酸 | C. | 铜 | D. | 乙醇 |
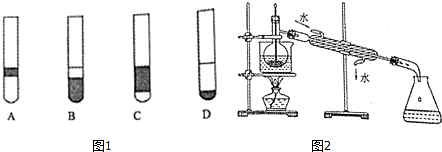
 下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后(溶质都有剩余),回答下列问题(不考虑溶液体积变化)
下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后(溶质都有剩余),回答下列问题(不考虑溶液体积变化)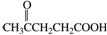 合成聚芳酯E的路线:
合成聚芳酯E的路线: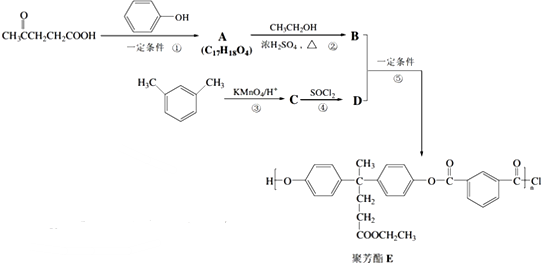
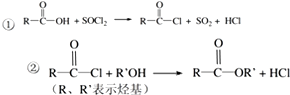
 .
. .
.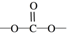 结构
结构 .
.