题目内容
9.如图,四种装置中所盛的溶液体积均为500mL,浓度均为0.6molL-1,(③可以实现铁表面镀锌)工作一段时间后,测得导线上均通过了0.2mol电子,此时溶液中的pH由大到小的顺序是( )
| A. | ④②①③ | B. | ④③①② | C. | ④③②① | D. | ①③②④ |
分析 ①③④是电解池,②是原电池,①中阳极上析出氧气,阴极上析出铜,所以电解质溶液酸性增强;②中正极上氢离子放电生成氢气,所以溶液的酸性减弱;③是电镀池,所以pH不变,④阳极上生成氯气,阴极上生成氢气,所以导致溶液中pH增大.
解答 解:①是电解CuSO4,电解方程式为:2H2O+2Cu2+$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+,根据方程式知生成4mol氢离子转移4mol电子,生成当转移0.2mol电子时氢离子浓度=$\frac{\frac{0.2mol}{4}×4}{0.5L}$=0.4mol/L;
②装置为原电池,铜电极上氢离子得电子生成氢气,根据2H++2e-═H2↑知,当转移0.2mol电子时溶液中氢离子浓度=0.6mol/L×2-$\frac{\frac{0.2mol}{2}×2}{0.5L}$=0.8mol/L;
③该装置实际上是一个电镀池,pH值不变,为强酸弱碱盐,溶液呈弱酸性;
④装置为电解NaCl饱和溶液,生成NaOH,为强碱溶液,pH值最大,所以pH大小顺序是④③①②,
故选:B.
点评 本题考查了原电池和电解池原理,明确离子放电顺序是解本题关键,结合化学反应方程式进行分析解答,难度中等.

练习册系列答案
相关题目
12.某温度下,物质X2SO4的饱和溶液密度为ρg•mL-1,c(X+)=c mol•L-1,溶质的质量分数为a%,溶质的摩尔质量为Mg•mol-1,溶解度为S g,下列表达式正确的是( )
| A. | c=$\frac{2000ρa}{M}$ | B. | a%=$\frac{c}{2000ρ}$ | C. | M=$\frac{1000ρa%}{c}$ | D. | $S=\frac{100cM}{2000ρ-cM}$ |
13.下列有关说法正确的是( )
| A. | 铁与稀盐酸制取氢气时,加入NaNO3固体或Na2SO4固体都不影响生成氢气的速率 | |
| B. | 加入反应物,则单位体积内活化分子百分数增大,化学反应速率增大 | |
| C. | 过程的自发性只能用于判断其方向性,不能确定其是否一定会发生和发生的速率 | |
| D. | 中和反应放热说明中和反应前后能量不守恒 |
10.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 植物油和溴水混合后振荡、静置 | 溶液分层,溴水褪色 | 植物油萃取了溴水中的Br2 |
| B | 将Cl2通入滴有酚酞NaOH的溶液 | 褪色 | Cl2具有漂白性 |
| C | 将过量的CO2通入CaCl2溶液 | 无白色沉淀生成 | 生成的Ca(HCO3)2可溶于水 |
| D | 将浓硫酸滴到胆矾晶体上 | 晶体逐渐变白色 | 浓硫酸的吸水性 |
| A. | A | B. | B | C. | C | D. | D |
4.对NO2与水的反应中下列说法中正确的是( )
| A. | 氧化剂与还原剂的物质的量之比为2:1 | |
| B. | 氧化产物与还原产物的物质的量之比为1:2 | |
| C. | 反应中若有6molNO2参与反应,有4mol电子转移 | |
| D. | 反应中NO2是氧化剂,水是还原剂 |
14.日常所用干电池其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2氧化吸收H2),电极反应可简化为:Zn-2e-═Zn2+、2NH4++2e-═2NH3+H2(NH3再用于结合Zn2+)根据上述叙述判断下列说法中正确的是( )
| A. | 干电池中Zn为正极,碳为负极 | |
| B. | 干电池可以实现化学能向电能的转化和电能向化学能的转化 | |
| C. | 干电池长时间连续使用时内装糊状物可能流出腐蚀电器 | |
| D. | 干电池工作时,电子由碳极经外电路流向Zn极 |
1.水是生命之源,下列关于水的说法正确的是( )
| A. | 水是弱电解质 | B. | 可燃冰是可以燃烧的水 | ||
| C. | 氢氧两种元素只能组成水 | D. | 0℃时冰的密度比液态水的密度大 |
18.下列物质的分子中既有σ键,又有π键的是( )
| A. | HCl | B. | H2O2 | C. | H2O | D. | N2 |
13.化学与生产生活密切相关,下列有关说法不正确的是( )
| A. | 富脂食品包装中常放入活性铁粉袋,以防止油脂氧化变质 | |
| B. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造晶体管 | |
| C. | Ni-Zn化合物的纳米颗粒可作 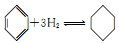 反应的催化剂,提高苯的转化率 反应的催化剂,提高苯的转化率 | |
| D. | 用K2FeO4代替Cl2处理饮用水时,既有杀菌消毒作用,又有净水作用 |