题目内容
工业上以NH3为原料制HNO3,将m g NH3完全转化为HNO3,且将生成的HNO3全部溶解于反应生成的水中,此硝酸溶液的质量分数为
- A.77.8%
- B.50%
- C.63.5%
- D.98%
A
据题可知所有NH3都形成HNO3,则
NH3+2O2====HNO3+H2O
则w(HNO3)=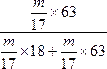 ×100%=77.8%。
×100%=77.8%。
据题可知所有NH3都形成HNO3,则
NH3+2O2====HNO3+H2O
则w(HNO3)=
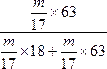 ×100%=77.8%。
×100%=77.8%。 
练习册系列答案
相关题目
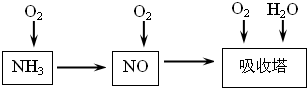
工业上以NH3为原料经过一系列反应可以得到HNO3。
(1)工业上NH3的催化氧化反应方程式为
;为了尽可能多地实现 向
向 的转化,请你提出一条可行性建议 。
的转化,请你提出一条可行性建议 。
(2)将工业废气NO与CO混合,经三元催化剂转化器处理如下:2CO+2NO 2CO2+N2。
2CO2+N2。
已知:
CO(g)+ 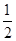 O2(g)=CO2(g)
△H=-283.0kJ·mol-1
O2(g)=CO2(g)
△H=-283.0kJ·mol-1
N2(g)+O2(g)=2NO(g) △H=+180.0kJ·mol-1
三元催化剂转化器中发生反应的热化学方程式为 ;
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度部分数据记录如下:
|
时间/s |
0 |
2 |
3 |
4 |
|
c(NO)/mol·L-1 |
1.00×10-3 |
1.50×10-4 |
1.00×10-4 |
1.00×10-4 |
|
|
|
|
|
|
①前2s内的平均反应速率v(CO)= ;
②在该温度下,反应的平衡常数K= ;
③假设在密闭容器中发生上述反应,达到平衡时下列措施能提高CO转化率的是
A.选用更有效的催化剂 B.恒容下充入Ar
C.适当降低反应体系的温度 D.缩小容器的体积
 C(CO)/mol·L-1
C(CO)/mol·L-1
 2.70×10-3
2.70×10-3