题目内容
12.某课外兴趣小组欲测定某 NaOH 溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数; 将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶 2~3 次;从碱式滴定管中放 入 25.00mL 待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入 0.1000mol/L 标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为 V1mL.
④重复以上过程.试回答下列问题:
(1)滴定结束时的现象为溶液由红色变为无色,并且30S内不变色
(2)滴定时边滴边摇动锥形瓶,眼睛应观察B
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是待测溶液润洗锥形瓶,若滴定过程中滴定管中有液体外漏于锥形瓶外由此造成的测定结果偏高,(填偏高、偏低或无影响)
(4)步骤②缺少的操作是用蒸馏水后再用标准溶液润洗2~3次.
分析 (1)根据滴定终点,锥形瓶中的溶液颜色发生变化,且半分钟内不褪色;
(2)根据滴定时眼睛应观察锥形瓶内溶液颜色的变化;
(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多;根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析误差;
(4)将酸式滴定管用蒸馏水洗净后,立即向其中注入标准稀溶液,则标准溶液的浓度偏小,所以要用标准溶液润洗.
解答 解:(1)用盐酸滴定氢氧化钠溶液以酚酞作指示剂,终点现象是当滴加最后一滴标准液时,溶液由红色变为无色,且30S内不变色;
故答案为:溶液由红色变为无色,并且30S内不变色;
(2)滴定时眼睛应观察锥形瓶内溶液颜色的变化,以判定终点的到达,故选B;
(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多,造成V(标准)偏大,c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(标准)偏高;
故答案为:待测溶液润洗锥形瓶;偏高;
(4)将酸式滴定管用蒸馏水洗净后,立即向其中注入标准稀溶液,则标准溶液的浓度偏小,所以缺少的操作为:用蒸馏水后再用标准溶液润洗2~3次;
故答案为:用蒸馏水后再用标准溶液润洗2~3次.
点评 本题主要考查了酸碱中和滴定的操作、误差分析等,难度中等,掌握中和滴定的原理是解题的关键.

练习册系列答案
相关题目
13.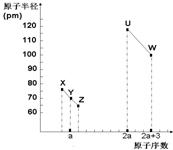 X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
 X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )| A. | U、X、W 三种元素最高价氧化物的水化物酸性依次增强 | |
| B. | 由Y、Z和氢三种元素形成的化合物中只有共价键 | |
| C. | XZ2、YZ2与X60的化学键类型和晶体类型都相同 | |
| D. | T元素与U同主族且在下一周期,能形成化合物TW4、TZ2、T3Y4 |
11.下列实验操作、现象与所得结论一致的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向盛有25mL沸水的烧杯中滴加5~6滴FeCl3饱和溶液,继续煮沸 | 溶液生成红褐色沉淀 | 制得Fe(OH)3胶体 |
| B | 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液, | 前者溶液变蓝, 后者有黄色沉淀 | KI3溶液中存在平衡: I3-?I2+I- |
| C | 将溴乙烷和NaOH乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液 褪色 | 一定产生了乙烯 |
| D | 在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液 | 溶液褪色 | CaCl2溶液有酸性 |
| A. | A | B. | B | C. | C | D. | D |
7.“碘钟”实验中,3I-+S2O${\;}_{8}^{2-}$═I${\;}_{3}^{-}$+2SO${\;}_{4}^{2-}$的反应速率可以用I${\;}_{3}^{-}$与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,得到的数据如下表:
回答下列问题:
(1)该实验的目的是:研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)根据①、②、⑤三个实验的数据,推测显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比.
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol/L | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O${\;}_{8}^{2-}$)/mol/L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
(1)该实验的目的是:研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)根据①、②、⑤三个实验的数据,推测显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比.
1.已知:C(s)+2NO(g)?N2(g)+CO2(g). T℃时.某研究小组向一恒容真空容器中充入NO和足量的碳单质,恒温条件下测得不同时间各物质的浓度如表.
(1)0~10min以V(NO)表示的平均反应速率为0.042mol/(L•min).
(2)根据表中数据,计算平衡时的NO转化率为60%.
(3)根据表中数据,计算T℃时该反应的平衡常数为0.56.
(4)30~35min改变的实验条件是分离出CO2.
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 35 | 0.32 | 0.34 | 0.15 |
(2)根据表中数据,计算平衡时的NO转化率为60%.
(3)根据表中数据,计算T℃时该反应的平衡常数为0.56.
(4)30~35min改变的实验条件是分离出CO2.