题目内容
雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al Mg、金属性Al Mg.(选填“>”、“<”、“=”)
(2)一种铝镍合金的结构如图 ,与其结构相似的化合物是 .
,与其结构相似的化合物是 .
A.氯化钠 B.氯化铯 C.石英 D.金刚石
(3)雷尼镍催化的一实例为:

化合物b中进行sp3杂化的原子有 (填元素符号)
(4)实验室检验Ni2+可用丁二酮肟与之作用生成红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为 .
②在配合物中画氢键、配位键 (已知 镍的配位数为4).

(1)元素第一电离能:Al
(2)一种铝镍合金的结构如图
 ,与其结构相似的化合物是
,与其结构相似的化合物是A.氯化钠 B.氯化铯 C.石英 D.金刚石
(3)雷尼镍催化的一实例为:

化合物b中进行sp3杂化的原子有
(4)实验室检验Ni2+可用丁二酮肟与之作用生成红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为
②在配合物中画氢键、配位键 (已知 镍的配位数为4).

考点:原子核外电子排布,配合物的成键情况,晶胞的计算,原子轨道杂化方式及杂化类型判断
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)Mg元素原子的3s能级容纳2个电子,为全满稳定状态,能量降低,同周期元素从左到右金属性逐渐减弱;
(2)由图可知铝镍合金的晶胞结构中,Ni原子数目为1,Al原子数目为8×
=1,为AlNi,每个Ni原子周围有8个Al原子,每个Al原子周围有8个Ni原子,据此结合选项中各物质的晶胞结构判断;
(3)苯环中存在大π键,碳原子杂化数为2,采取sp2杂化,侧链中C、O、N原子根据成的单键数目与孤对电子确定杂化轨道数目判断杂化方式;
(4)①根据核外电子排布规律书写;
②Ni2+含有空轨道,N原子含有孤对电子对,N原子与Ni2+形成配位键,氧原子与氢原子之间形成氢键.
(2)由图可知铝镍合金的晶胞结构中,Ni原子数目为1,Al原子数目为8×
| 1 |
| 8 |
(3)苯环中存在大π键,碳原子杂化数为2,采取sp2杂化,侧链中C、O、N原子根据成的单键数目与孤对电子确定杂化轨道数目判断杂化方式;
(4)①根据核外电子排布规律书写;
②Ni2+含有空轨道,N原子含有孤对电子对,N原子与Ni2+形成配位键,氧原子与氢原子之间形成氢键.
解答:
解:(1)Mg元素原子的3s能级容纳2个电子,为全满稳定状态,能量降低,第一电离能高于同周期相邻的元素,故第一电离能Al<Mg,
同周期元素从左到右金属性逐渐减弱,因此金属性Al<Mg,
故答案为:<;<;
(2)由图可知铝镍合金的晶胞结构中,Ni原子数目为1,Al原子数目为8×
=1,为AlNi,每个Ni原子周围有8个Al原子,每个Al原子周围有8个Ni原子,
A.氯化钠中每个钠离子周围有6个氯离子,每个氯离子周围有6个钠离子,不符合;
B.氯化铯中每个铯离子周围有8个氯离子,每个氯离子周围有8个铯离子,符合;
C.石英为空间立体网状结构,硅原子周围有4个氧原子,氧原子周围有2个硅原子,不符合;
D.金刚石为空间立体网状结构,每C原子周围有4个C原子,不符合;
故答案为:B;
(3)苯环中存在大π键,碳原子杂化数为2,采取sp2杂化,侧链中C原子成4个单键,杂化轨道数为4,采取sp3杂化,O原子成2个单键,含有2对孤对电子,杂化轨道数为4,采取sp3杂化,N原子成3个单键,含有1对孤对电子,杂化轨道数为4,采取sp3杂化,
故答案为:C、N、O;
(4)①Ni是28号元素,核外有28个电子,其原子核外电子排布为1s22s22p63s23p63d84s2,
故答案为:1s22s22p63s23p63d84s2;
②Ni2+含有空轨道,N原子含有孤对电子对,N原子与Ni2+形成配位键,不同分子中氧原子与氢原子之间形成氢键,如图所示: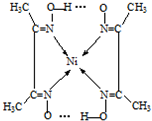 ,
,
故答案为: .
.
同周期元素从左到右金属性逐渐减弱,因此金属性Al<Mg,
故答案为:<;<;
(2)由图可知铝镍合金的晶胞结构中,Ni原子数目为1,Al原子数目为8×
| 1 |
| 8 |
A.氯化钠中每个钠离子周围有6个氯离子,每个氯离子周围有6个钠离子,不符合;
B.氯化铯中每个铯离子周围有8个氯离子,每个氯离子周围有8个铯离子,符合;
C.石英为空间立体网状结构,硅原子周围有4个氧原子,氧原子周围有2个硅原子,不符合;
D.金刚石为空间立体网状结构,每C原子周围有4个C原子,不符合;
故答案为:B;
(3)苯环中存在大π键,碳原子杂化数为2,采取sp2杂化,侧链中C原子成4个单键,杂化轨道数为4,采取sp3杂化,O原子成2个单键,含有2对孤对电子,杂化轨道数为4,采取sp3杂化,N原子成3个单键,含有1对孤对电子,杂化轨道数为4,采取sp3杂化,
故答案为:C、N、O;
(4)①Ni是28号元素,核外有28个电子,其原子核外电子排布为1s22s22p63s23p63d84s2,
故答案为:1s22s22p63s23p63d84s2;
②Ni2+含有空轨道,N原子含有孤对电子对,N原子与Ni2+形成配位键,不同分子中氧原子与氢原子之间形成氢键,如图所示:
 ,
,故答案为:
 .
.
点评:本题考查知识点有电离能、杂化轨道、化学键、核外电子排布规律等,涉及的知识点较多,题目综合性较强,难度中等.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
下列物质中,不能直接用单质反应制得的是( )
| A、Cu2S |
| B、SO2 |
| C、FeCl2 |
| D、NO |
某元素原子的第4电子层有3个电子,则第3电子层的电子数有( )
| A、2 | B、8 | C、10 | D、18 |
某元素的原子3d能级上有1个电子,它的N能层上电子数是( )
| A、0 | B、2 | C、5 | D、8 |
具有下列最外层电子排布的基态原子,其相应的元素,一定属于主族的是( )
| A、ns1 |
| B、ns2 |
| C、ns2np6 |
| D、ns2np2 |
39号元素钇的电子排布式应是下列排布中的哪一种( )
| A、1s22s22p63s23p63d104s24p64d15s2 |
| B、1s22s22p63s23p63d104s24p65s25p1 |
| C、1s22s22p63s23p63d104s24p64f15s2 |
| D、1s22s22p63s23p63d104s24p65s25d1 |
下列病患是由于缺乏维生素D引起的是( )
| A、坏血病 | B、佝偻病 |
| C、贫血 | D、呆小症 |
