题目内容
有关物质存在如下图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.

请回答下列问题;
(1)反应①的化学方程式为 ;
(2)反应②的离子方程式为 ;
(3)写出另外一种实验室制取H的化学方程式 ;
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀.此沉淀的Ksp=7.1×10-9mol?L-3.将0.01mol?L-1的D溶液与0.001mol?L-1的Pb(NO3)2溶液等体积混合,你认为能否形成沉淀 (填“能”或“不能”),请通过计算说明.

请回答下列问题;
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)写出另外一种实验室制取H的化学方程式
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀.此沉淀的Ksp=7.1×10-9mol?L-3.将0.01mol?L-1的D溶液与0.001mol?L-1的Pb(NO3)2溶液等体积混合,你认为能否形成沉淀
考点:无机物的推断
专题:推断题
分析:G为紫黑色固体单质,则G为I2,C为气体单质,则C具有氧化性,D中含有I-,C由浓A溶液与B在加热下生成,由B在制取气体H中做催化剂,推出B应为MnO 2,则A为HCl,C为Cl 2,实验室中用MnO2催化制取的气体是O2,即H为O 2,E为固体,则E是KClO3,所以F为KCl,在酸性条件下KClO 3可以将I-氧化为I2,结合元素化合物的性质和题目要求可解答该题.
解答:
解:G为紫黑色固体单质,则G为I 2,C为气体单质,则C具有氧化性,D中含有I-,C由浓A溶液与B在加热下生成,由B在制取气体H中做催化剂,推出B应为MnO 2,则A为HCl,C为Cl 2,实验室中用MnO2催化制取的气体是O2,即H为O 2,E为固体,则E是KClO3,所以F为KCl,在酸性条件下KClO 3可以将I-氧化为I2,
(1)由以上分析可知B是MnO2,A是HCl,C是Cl2.发生反应的化学方程式是4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O,
故答案为:4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O;
(2)反应②是KI、KClO3与浓盐酸的反应,在酸性条件下KClO 3可以将I-氧化为I2,反应的离子方程式为6I-+ClO3-+6H+=3I2+Cl-+3H2O,
故答案为:6I-+ClO3-+6H+=3I2+Cl-+3H2O;
(3)实验室制取氧气的化学反应还有:2H2O2
2H2O+O2↑或2KMnO4
K2MnO4+MnO2+O2↑,
故答案为:2H2O2
2H2O+O2↑或2KMnO4
K2MnO4+MnO2+O2↑;
(4)Q=c(Pb2+)?c(I-)2=
×0.001×(
×0.01)2=1.25×10-8>7.0×10-9,可以生成PbI2沉淀,故答案为:能.
(1)由以上分析可知B是MnO2,A是HCl,C是Cl2.发生反应的化学方程式是4HCl(浓)+MnO2
| ||
故答案为:4HCl(浓)+MnO2
| ||
(2)反应②是KI、KClO3与浓盐酸的反应,在酸性条件下KClO 3可以将I-氧化为I2,反应的离子方程式为6I-+ClO3-+6H+=3I2+Cl-+3H2O,
故答案为:6I-+ClO3-+6H+=3I2+Cl-+3H2O;
(3)实验室制取氧气的化学反应还有:2H2O2
| ||
| ||
故答案为:2H2O2
| ||
| ||
(4)Q=c(Pb2+)?c(I-)2=
| 1 |
| 2 |
| 1 |
| 2 |
点评:本题考查元素化合物的推断,侧重于学生的分析能力和计算能力的考查,为高考常见题型,题目难度中等,本题涉及氧化还原反应原理、溶度积等的计算具有一定的综合性,注意根据物质的特性作为该推断题的突破口.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
下列离子方程式与所述事实相符且正确的是( )
| A、用亚硫酸钾溶液吸收硫酸工业尾气中的SO2:SO2+SO32-+H20=2HSO3- |
| B、向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| C、高锰酸钾与足量浓盐酸反应制氯气:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O |
| D、漂白粉溶液中,通入过量的二氧化碳:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A、足量的Fe在1molCl2中充分燃烧,转移的电子数为2NA |
| B、在标准状况下,11.2L NO与11.2L O2混合后其原子总数为2NA |
| C、在O℃101.1kpa条件下,22.4L的乙烷中含有共价键的数目为6NA |
| D、铜、锌和稀硫酸构成原电池,当转移电子数为NA时,产生气体的分子数为0.5NA |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1mol羟基与17gNH3所含电子数都为NA |
| B、12.4g白磷(分子式为P4)中含有P-P共价键0.6NA |
| C、常温常压下,Na2O2与足量H2O反应,生成了0.2molO2,转移电子的数目为0.8 NA |
| D、适量铜粉溶解于1L0.5mol?L-1稀硝酸中,当生成2.24LNO时,溶液中氮原子数为0.4 NA |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、15.6 g Na2O2与过量CO2反应时,转移电子数为0.4NA |
| B、5.6 g Fe与过量硫粉反应,转移电子数为0.3NA |
| C、3.1 g白磷与红磷的混合物中所含磷原子数为0.1NA |
| D、某温度时,pH=6的纯水中含10-6NA个OH- |
常温下将NaOH稀溶液与CH3COOH稀溶液混合,不可能出现的结果是( )
| A、pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| B、pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| C、pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| D、pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
下列反应的离子方程式书写正确的是( )
| A、在澄清石灰水中加入少量小苏打:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| B、苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| C、将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、将标准状况下112mL氯气通入10mL浓度为1mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2═3Fe3++6Cl-+2Br2 |
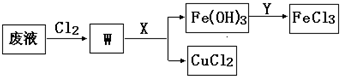 我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用.
我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用.