题目内容
19.下列离子方程式书写正确的是( )| A. | 氯化铝与氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 稀硫酸与氢氧化钡溶液反应:H++OH-+Ba2++SO42-═H2O+BaSO4↓ | |
| C. | 碳酸钙与稀盐酸反应:CO32--+2H+═H2O+CO2↑ | |
| D. | 向苏打溶液中加入足量的醋酸:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- |
分析 A.反应生成氢氧化铝和氯化铵;
B.不符合离子的配比;
C.碳酸钙在离子反应中保留化学式;
D.反应生成醋酸钠、水、二氧化碳.
解答 解:A.氯化铝与氨水反应的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A错误;
B.稀硫酸与氢氧化钡溶液反应的离子反应为2H++2OH-+Ba2++SO42-═2H2O+BaSO4↓,故B错误;
C.碳酸钙与稀盐酸反应的离子反应为CaCO3-+2H+═Ca2++H2O+CO2↑,故C错误;
D.向苏打溶液中加入足量的醋酸的离子反应为CO32-+2CH3COOH═CO2↑+H2O+2CH3COO-,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质及电荷守恒,题目难度不大.

练习册系列答案
相关题目
9.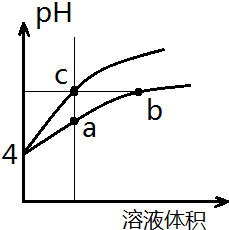 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )| A. | a、c两点溶液的导电能力相同 | |
| B. | b点溶液中c(H+)=c(OH-)+c(NH3•H2O) | |
| C. | a、b、c三点溶液水的电离程度a>b>c | |
| D. | 用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc |
7.下列物质中属于碱的是( )
| A. | KNO3 | B. | O3 | C. | Ca(OH)2 | D. | HNO3 |
4.醋酸溶液中存在电离平衡:CH3COOH═CH3COO-+H+,下列叙述不正确的是( )
| A. | CH3COOH溶液中离子浓度的关系满足:c(H+)>c(CH3COO-) | |
| B. | CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动 | |
| C. | 0.1mol/L的CH3COOH溶液加水稀释,溶液中的离子浓度均减小 | |
| D. | 常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH=7 |
11.下列说法正确的是( )
| A. | BaSO4难溶于水,但BaSO4是电解质 | |
| B. | 铜和石墨均能导电,所以它们都是电解质 | |
| C. | 电解质一定能导电,能导电的物质不一定属于电解质 | |
| D. | 液态HCl不导电,所以HCl不是电解质 |
9.一氧化碳、氢气都是重要的化工原料,又可作为燃料.生产水煤气(主要成分为CO和H2)过程中发生的主要反应如下:①C(g)+CO2(g)?2CO(g)△H1
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2
③C(s)+H2O(g)?CO(g)+H2(g)△H3
回答下列问题:
则△H2=(a+2b-c-2d)kJ•mol-1kJ.mol-1(用含a,b,c,d字母的代数式表示).
(2)反应③的化学平衡常数K的表达式为K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$;上述反应中△H1、△H2、△H3之间的关系为△H3=△H1+△H2.
(3)不同温度下反应②的平衡常数如下表所示,则△H2<0(填“<”或“>”)
500℃时,若起始时密闭容器中充有物质的量浓度均为0.02mol•L-1的CO和H2O.则反应②达到化学平衡时CO的转化率为75%.
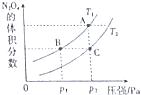
(4)对于反应2NO2(g)?N2O4(g)△H<0,当温度为T1、T2时,平衡体系中的体积分数随压强变化的曲线如图所示,则T1<T2(填“<”或“>”);压强增大,平衡向正(填“正”或“逆”)反应方向移动,B、C两点的平衡常数B>C(填“>”、“<”或“=”)
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2
③C(s)+H2O(g)?CO(g)+H2(g)△H3
回答下列问题:
| 化学键 | C≡O | H-O | H-H | C═O |
| E/(kJ.mol-1) | a | b | c | d |
(2)反应③的化学平衡常数K的表达式为K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$;上述反应中△H1、△H2、△H3之间的关系为△H3=△H1+△H2.
(3)不同温度下反应②的平衡常数如下表所示,则△H2<0(填“<”或“>”)
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)对于反应2NO2(g)?N2O4(g)△H<0,当温度为T1、T2时,平衡体系中的体积分数随压强变化的曲线如图所示,则T1<T2(填“<”或“>”);压强增大,平衡向正(填“正”或“逆”)反应方向移动,B、C两点的平衡常数B>C(填“>”、“<”或“=”)