题目内容
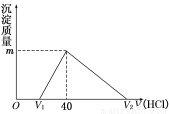
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下图所示,其中R与T原子序数之和为20,下列判断正确的是
|
| R |
| |
T | Q |
| W | G |
A.离子半径:T> W
B.最高价氧化物对应水化物的酸性:Q >W>G
C.最简单气态氢化物的热稳定性:Q < R
D.T和G组成的化合物甲溶于水,其水溶液呈中性
C
【解析】
试题分析:设R的原子序数为x,则T、Q、W、G的原子序数分别为x+6、x+7、x+9、x+10,则x+x+6=20,解得x=7,则R、T、Q、W、G分别为N、Al、Si、S、Cl。A、离子半径:Al3+<S2?,故A错误;B、最高价氧化物对应水化物的酸性:H2SiO3<H2SO4<HClO4,故B错误;C、最简单气态氢化物的热稳定性:SiH4<NH3,故C正确;D、T和G组成的化合物甲为AlCl3,其水溶液呈酸性,故D错误。
考点:本题考查元素的推断、元素周期律。

A、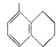 所有碳原子可能在同一平面上 所有碳原子可能在同一平面上 | B、 一氯代物有4种 一氯代物有4种 | C、 的命名为:2-甲基-1-丙醇 的命名为:2-甲基-1-丙醇 | D、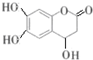 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
(10分)2010年8月7日,甘肃甘南藏族自治州舟曲县发生特大泥石流,造成大量人员伤亡,其中饮用水安全在灾后重建中占有极为重要的地位,某研究小组提取三处被污染的水源进行了如下分析:并给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E五种常见化合物都是由下表中的离子形成的:
阳离子 | K+、Na+、Cu2+、Al3+ |
阴离子 | SO |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液.
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解.
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃).
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验现象写出下列物质化学式:A B C D E

 表示的有机物中,能发生消去反应的共有
表示的有机物中,能发生消去反应的共有 、HCO
、HCO 、NO
、NO