题目内容
9.将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判断合理的是( )| A. | Fe(NO3)x中的x为2 | |
| B. | 稀HNO3在反应中只表现氧化性 | |
| C. | 反应中每还原0.4 mol氧化剂,就有1.2 mol电子被转移 | |
| D. | 磁性氧化铁中的铁元素全部被氧化 |
分析 3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O中Fe元素的化合价由+2价升高为+3价,N元素的化合价由+5价降低为+2价,以此来解答.
解答 解:A.由N原子守恒可知,Fe(NO3)x中的x为3,故A错误;
B.生成NO体现硝酸的氧化性,生成盐体现其酸性,故B错误;
C.反应中每还原0.4 mol氧化剂,由N元素的化合价变化可知,就有0.4mol×(5-2)=1.2 mol电子被转移,故C正确;
D.磁性氧化铁中Fe元素的化合价为+2、+3价,则部分铁元素被氧化,故D错误;
故选C.
点评 本题考查氧化还原反应,为高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应基本概念,题目难度不大.

练习册系列答案
相关题目
20.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
| A. | 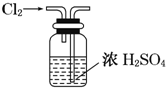 干燥Cl2 | B. | 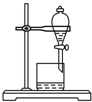 分离乙醇和乙酸 | ||
| C. | 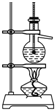 石油的蒸馏 | D. | 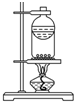 分离I2 |
17.去甲肾上腺素可以调控动物机体的植物性神经功能.其结构简式如图所示.下列说法正确的是( )

| A. | 每个去甲肾上腺素分子中含有 3 个酚羟基 | |
| B. | 去甲肾上腺素分子难溶于水 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
4.下列实验的反应原理用离子方程式表示正确的是( )
| A. | 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3•H2O+H3O+ | |
| B. | 将16.8g铁粉投入100mL4.0mol/L的HNO3溶液中(还原产物只有NO):6Fe+20H++5NO3-=3Fe2++3Fe3++5NO↑+10H2O | |
| C. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O | |
| D. | 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
14.下列离子在溶液中能大量共存,且溶液加入镁粉有气体产生的是( )
| A. | Ba2+、Na+、NO3-、I- | B. | H+、Ag+、NO3-、HCO3- | ||
| C. | Fe3+、Na+、S2-、Cl- | D. | Al3+、K+、Br-、SO42- |
1.下列说法不正确的是( )
| A. | 煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料 | |
| B. | 石油分馏得到的汽油、煤油、柴油等各种沸点范围不同的混合物 | |
| C. | 通过石油裂化和裂解可以获得轻质油和重要化工原料(乙烯、丙烯等) | |
| D. | 天然气和沼气的主要成分是甲烷,它们都属于不可再生能源 |
18.下列分子中,既含有σ键又含有π键的是( )
| A. | CH4 | B. | N2 | C. | HCl | D. | F2 |
 元素在周期表中的位置,反映了元素的原子结构和元素性质.图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素性质.图是元素周期表的一部分.