题目内容
18.将下列各组物质按酸、碱、盐分类排序正确的是( )| A. | 硫酸、纯碱、石灰石 | B. | 硝酸、烧碱、胆矾 | ||
| C. | 醋酸、碱式碳酸铜、醋酸钠 | D. | 盐酸、熟石灰、苛性钠 |
分析 酸是指电离时生成的阳离子全部是氢离子的化合物.
碱是指电离时生成的阴离子全部是氢氧根离子的化合物.
盐是指由金属离子或铵根离子和酸根离子组成的化合物.
解答 解:A.硫酸属于酸,纯碱、石灰石属于盐,故A错误;
B.硝酸属于酸,烧碱属于碱,醋酸钠属于盐,故B正确;
C.醋酸属于酸,碱式碳酸铜、醋酸钠属于盐,故C错误;
D.磷酸属于酸,熟石灰是氧化钙,属于氧化物,苛性钠属于碱,故D错误.
故选B.
点评 本题考查了物质类别的判别,题目难度不大,解答本题要充分理解酸碱盐的概念的含义,只有这样才能对各种物质进行正确的分类.

练习册系列答案
相关题目
8.以下气体因与人体血液中血红蛋白作用引起中毒的是( )
| A. | CO2 | B. | CO | C. | O2 | D. | SO2 |
9.为了使Al2(SO4)3中的Al3+完全沉淀,适宜用到的试剂是( )
| A. | NaOH溶液 | B. | Ba(OH)2溶液 | C. | 氨水 | D. | BaCl2溶液 |
6.大气污染的危害是多方面的,它既危害人体健康,又影响动植物的生长,严重时会影响地球的气候.2016年1月5日,常德市pM2.5为425,“勇夺”全国526个城市亚军.下列现象并非大气污染导致( )
| A. | 形成酸雨 | B. | 使全球气候变暖 | C. | 破坏臭氧层 | D. | 产生雷电 |
13.有关FeSO4溶液的说法正确的是( )
| A. | 溶液为浅绿色 | |
| B. | 溶液为棕黄色 | |
| C. | 加入硫氰化钾溶液显红色 | |
| D. | 滴加NaOH溶液,产生白色沉淀,该沉淀放置在空气中不变色 |
3.设阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 标准状况下,11.2 L CCl4所含的分子数为0.5 NA | |
| B. | 常温常压下,4.2 g C2H4和C8H16的混合物中含有的碳原子数为0.3 NA | |
| C. | 7.8 g苯分子中碳碳双键的数目为0.3 NA | |
| D. | 6.4 g Cu与20 mL 10 mol•L-1浓硫酸反应,转移的电子数为0.2 NA |
10.雾霾天气对大气环境、人体健康、交通安全都带来了不利影响,因此引起了人们的高度重视.下列有关雾霾的叙述中不正确的是( )
| A. | 霾是一种分散系,分散质是固体 | |
| B. | 雾是一种分散系,分散剂是气体 | |
| C. | 霾属于胶体分散系 | |
| D. | 减少生产生活中产生的扬尘可以减少雾霾天气的形成 |
3.下列叙述正确的是( )
| A. | 同温同压下,两种气体的体积之比等于摩尔质量之比 | |
| B. | 同温同压下,两种气体的物质的量之比等于密度之比 | |
| C. | 同温同压下,两种气体的摩尔质量之比等于密度之比 | |
| D. | 同温同容下,两种气体的质量之比等于压强之比 |
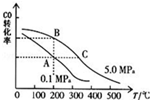 甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题