题目内容
6.构成原电池的条件(1)有两个活泼性不同的电极
(2)将电极插入电解质溶液中
(3)两电极间构成闭合回路
(4)能自发的进行氧化还原反应.
分析 构成原电池需具备以下条件:两个活性不同的电极;电解质溶液;形成闭合回路;存在能自动发生的氧化还原反应,且为放热反应,以此来解答.
解答 解:原电池的构成条件是:1、有两个活泼性不同的电极,2、将电极插入电解质溶液中,3、两电极间构成闭合回路,4、能自发的进行氧化还原反应;原电池中正极上发生还原反应,负极上发生氧化反应,
故答案为:(1)有两个活泼性不同的电极;
(2)将电极插入电解质溶液中;
(3)两电极间构成闭合回路;
(4)能自发的进行氧化还原反应.
点评 本题考查了原电池原理的分析应用,该题是高考中的常见考点,属于基础性试题的考查,难度不大.明确原电池的工作原理、构成条件是答题的关键.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
16.关于化学键的叙述中,正确的是( )
| A. | HCl电离产生H+和 Cl-,可判断HCl分子中存在离子键 | |
| B. | NaHSO4固体中含有的阴离子与阳离子的个数比为1:1 | |
| C. | 化学键是指使原子或离子相互结合的静电吸引作用力 | |
| D. | 不同元素组成的多原子分子中的化学键一定全是极性键 |
17.高温下硫酸亚铁发生如下反应:2FeSO4=Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钙溶液中,得到的沉淀是( )
| A. | CaSO4和CaSO3 | B. | CaSO4 | C. | CaS | D. | CaSO3 |
14.类比是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中,正确的是( )
| A. | IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| B. | CH4是正四面体结构,则SiH4也是正四面体结构 | |
| C. | 锂与氧气反应:4Li+O2═2 Li2O,则钠与氧气反应:4Na+O2═2Na2O | |
| D. | CaCO3与稀硝酸反应生成CO2,则CaSO3与稀硝酸反应生成SO2 |
1.把a、b、c、d 4块金属浸入稀硫酸中,用导线两两相连组成原电池.若把a、b相连时,a为负极;若a、c相连时,电流由c经导线流向a; b、d相连时,电子经由导线由d流向b,则四种金属的活动顺序由强到弱的顺序是( )
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>a>c>d |
18.家庭烹饪时,同时加酒和醋,烹饪出的菜更可口,这是因为有( )
| A. | 生成盐类物质 | B. | 生成酸类物质 | C. | 生成酯类物质 | D. | 生成醇类物质 |
15.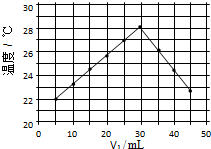 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )| A. | 做该实验时环境温度为22℃ | |
| B. | 该实验表明化学能可能转化为热能 | |
| C. | NaOH溶液的浓度约为1.5mol/L | |
| D. | 该实验表明有水生成的反应都是放热反应 |
16.某有机物的结构简式为 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成 ②水解 ③酯化 ④氧化 ⑤消去.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤消去.
| A. | ①③④ | B. | ①③④⑤ | C. | ②③④ | D. | ①③⑤ |