题目内容
19.如图是由常见元素组成的一些单质及其化合物之间的转化关系图.各方框表示有关的一种反应物或生成物(部分物质已经略去).其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体.
(1)写出C→E的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,干燥C常用碱石灰(填写试剂名称).
(3)E物质遇到D物质时,会观察到无色气体变为红棕色现象,若用排水法收集F,则最终集气瓶中收集到的气体为NO(填写物质的化学式).
(4)写出A→D的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
分析 无色无味气体A与过氧化钠反应的得到气体D,则A为CO2,D为O2,C是使湿润的红色石蕊试纸变蓝的气体,应为NH3,氢气与B反应生成C,则B为N2,氨催化氧化生成E为NO,NO与氧气反应生成F为NO2,G与Cu反应可以得到NO或二氧化氮,则G为HNO3,M是最常见的无色液体,与二氧化氮反应得到硝酸,则M为H2O,据此解答.
解答 解:无色无味气体A与过氧化钠反应的得到气体D,则A为CO2,D为O2,C是使湿润的红色石蕊试纸变蓝的气体,应为NH3,氢气与B反应生成C,则B为N2,氨催化氧化生成E为NO,NO与氧气反应生成F为NO2,G与Cu反应可以得到NO或二氧化氮,则G为HNO3,M是最常见的无色液体,与二氧化氮反应得到硝酸,则M为H2O,
(1)C→E的反应为氨的催化氧化,反应的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)实验室常用加热氯化铵和氢氧化钙两种固体混合物的方法制备物质氨气,其化学方程式为:2 NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,干燥C常用 碱石灰,
故答案为:2 NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;碱石灰;
(3)E为NO,E物质遇到空气时,会观察到 无色气体变为红棕色现象,若用排水法收集F,则最终集气瓶中收集到的气体为 NO,
故答案为:无色气体变为红棕色; NO;
(填写物质的化学式).
(4)A→D的反应为过氧化钠与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2.
点评 本题考查无机物的推断,涉及N、Na元素化合物知识,侧重于元素化合物知识的考查,C和M的性质及A能与过氧化钠反应是推断突破口,难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 烧碱溶液盛装在带有玻璃塞的试剂瓶中 | |
| B. | 少量金属钠保存在煤油中 | |
| C. | 向紫色石蕊试液中加入新制氯水,石蕊试液先变红后褪色 | |
| D. | 常温下可用铁、铝制容器来盛装浓硝酸或浓硫酸 |
| A. | 铜和硝酸反应 | B. | 锌和氯化铁溶液反应 | ||
| C. | 细铁丝在氯气中燃烧 | D. | 氯化铝与氢氧化钠溶液反应 |
| A. | 物质失去的电子数越多,其还原性越强 | |
| B. | 物质所含元素化合价升高的反应叫还原反应 | |
| C. | 某元素由化合态变为游离态,则它一定被还原 | |
| D. | 置换反应一定属于氧化还原反应 |
| A. | Na+、Cu2+、Cl-、OH- | B. | K+、Ca2+、HCO3-、OH- | ||
| C. | Fe2+、H+、SO42-、NO3- | D. | Na+、CO32-、OH-、K+ |
| A. | 链状有机物C5H7Cl,其结构中肯定含一个碳碳双键 | |
| B. | C8H10是苯的同系物,它共有3中不同的结构 | |
| C. | 聚氯乙烯(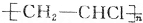 )的相对分子质量一定比聚乙烯( )的相对分子质量一定比聚乙烯( )的大34.5n )的大34.5n | |
| D. | 可用银氨溶液区别葡萄糖和果糖 |
| A. | 元素的原子半径:A<B<C<D<E | |
| B. | 对应氢化物的热稳定性:D>E | |
| C. | B与C、B与D形成的化合物中化学键类型相同 | |
| D. | 五种元素中最高价氧化物对应的水化物酸性最强的是E |

| A. | (2) | B. | (4) | C. | (3) | D. | (5) |
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 生石灰能与水反应,可用来干燥氯气 | |
| D. | 二氧化硅不与强酸反应,可用石英作为反应容器制取氢氟酸 |