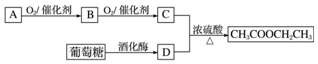
题目内容
12.据报导,我国已研制出“可充室温钠一二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠一四甘醇二甲醚,电池总反应为:4Na+3CO2 $?_{充电}^{放电}$2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上.下列叙述不正确的是( )| A. | 放电时钠金属片发生氧化反应 | |
| B. | 充电时碳纳米管接直流电源的正极 | |
| C. | 放电时每消耗3molCO2,转移12 mol电子 | |
| D. | 充电时的阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+ |
分析 由4Na+3CO2 $?_{充电}^{放电}$2Na2CO3+C可知,放电为原电池反应,Na为负极失去电子,正极上C得到电子;充电为电解池,阳极与正极相连,阳极失去电子发生氧化反应,以此来解答.
解答 解:A.放电时钠金属片,作负极,失去电子发生氧化反应,故A正确;
B.原电池中正极上C得到电子,则充电时碳纳米管接直流电源的正极,故B正确;
C.放电时每消耗3molCO2,4molNa失去电子,转移4 mol电子,故C错误;
D.充电为电解池,阳极与正极相连,阳极失去电子发生氧化反应,则阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+,故D正确;
故选C.
点评 本题考查原电池及电解池,为高频考点,把握电极判断、电极反应、工作原理为解答的关键,侧重分析与应用能力的考查,注意电化学知识的应用,题目难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
18.下列分子中所有碳原子肯定不在同一平面上的是( )
| A. | 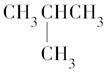 | B. | CH3CH=CHCH3 | C. | CH2=CHCH2CH3 | D. | 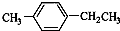 |
3.当足量的CO通过玻璃管内灼热的某一氧化物后,充分反应,管内物质质量减少了27.5%,则氧化物为( )
| A. | CuO | B. | MnO2 | C. | Fe2O3 | D. | Fe3O4 |
7.下列有关说法正确的是( )
| A. | 明矾既可用作净水剂,也可用作消毒剂 | |
| B. | 小苏打、氢氧化铝都可用于治疗胃酸过多 | |
| C. | 煤的干馏、石油的分馏都属于化学变化 | |
| D. | 已知PM2.5是指大气中直径小于或等于2.5微米(1微米=1000纳米)的颗粒物,则PM2.5在空气中能形成胶体 |
17.短周期W、X、Y、Z四种元素的子序数依次增大.W的某种原子无中子,X、Y可形成原子个数比为1:1的具有漂白性的物质,工业上常用电解熔融的YZ来获得Y的单质.下列说法正确的是( )
| A. | X、Y形成的原子个数比为1:1的漂白性物质中既有极性共价键又有非极性共价键 | |
| B. | 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W) | |
| C. | W与X形成的化合物的熔沸点高于W与Z形成的化合物的熔沸点 | |
| D. | X、Y、Z三种元素形成的化合物,其水溶液一定呈碱性 |
2.下列反应能用离子方程式CO32-+2H+→CO2↑+H2O表示的是( )
| A. | 石灰石与足量盐酸反应 | B. | 碳酸钠与足量盐酸反应 | ||
| C. | 碳酸钠与足量醋酸反应 | D. | 碳酸钡与足量硝酸反应 |