题目内容
3.下各项性质的比较中不正确的是( )| A. | 原子半径:C<N<O<F | B. | 最高正化合价:Si<P<S<Cl | ||
| C. | 热稳定性:GeH4<SiH4<CH4 | D. | 酸性:H3CO3<H2SiO3<Ge(OH)4 |
分析 A.同一周期中,原子序数越大,原子半径越小;
B.四种元素位于同一周期,最外层电子数逐渐增多,最高化合价逐渐增大;
C.非金属性越强,对应氢化物的稳定性越强;
D.非金属性越强,最高价氧化物对应水合物的酸性越强.
解答 解:A.C、N、O、F位于第二周期,原子序数逐渐增大,原子半径逐渐减小,则原子半径大小为:C>N>O>F,故A错误;
B.Si、P、S、Cl位于第三周期,最外层电子数逐渐增多,最高正化合价逐渐增大,则最高化合价大小为:Si<P<S<Cl,故B正确;
C.非金属性:Ge<Si<C,则氢化物的热稳定性为:GeH4<SiH4<CH4,故C正确;
D.非金属性:Ge<Si<C,则最高价氧化物对应水合物的酸性强弱:H3CO3<H2SiO3<Ge(OH)4,故D正确;
故选A.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律内容为解答关键,注意熟练掌握判断金属性、氢化物稳定性、最高价含氧酸的酸性强弱的方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
14.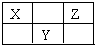 X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
 X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
X、Y、Z三种短周期元素在周期表中的位置如图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )| A. | 原子序数由大到小为 Z>Y>X | |
| B. | 氢化物最稳定的元素为Z | |
| C. | 最高价氧化物的水化物酸性最强的元素为Z | |
| D. | 原子半径由大到小为 Y>Z>X |
11.下列现象与氢键有关的是( )
①HF的熔、沸点比HCl的熔、沸点高②NH3极易溶于水③冰的密度比液态水的密度小④水分子高温下很稳定.
①HF的熔、沸点比HCl的熔、沸点高②NH3极易溶于水③冰的密度比液态水的密度小④水分子高温下很稳定.
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ①③ |
18.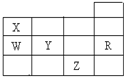 如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | 元素原子半径:W<Y | |
| B. | X、Y的阴离子电子层结构都与R原子相同 | |
| C. | Y元素的非金属性比W元素的非金属性强 | |
| D. | 常温常压下五种元素的单质中,Z单质的沸点最高 |
15.盐酸与块状CaCO3反应时,不能使反应的最初速率明显加快的是( )
| A. | 将盐酸的用量增加一倍 | B. | 盐酸的浓度增加一倍,用量减半 | ||
| C. | 温度升高30℃ | D. | 改用更小块的CaCO3 |
12.下列变化属于物理变化的是( )
| A. | O2在放电条件下变成O3 | B. | 加热胆矾成无水硫酸铜 | ||
| C. | 漂白的草帽久置于空气中变黄 | D. | 石油分馏 |
13.实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液
(2)配制时,其正确的操作顺序是B、C、A、F、E、D(用字母表示,每个字母只能用一次).
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻线2-3cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶.
(4)若出现如下情况,对所配溶液浓度将有何影响?(填偏大、偏小、不变),没有进行A操作时浓度偏小;加蒸馏水时不慎超过了刻度线时浓度偏小;定容时俯视时浓度偏大.
(1)配制250mL0.1mol/L的盐酸溶液
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶、烧杯外还需要的其它玻璃仪器 |
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻线2-3cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶.
(4)若出现如下情况,对所配溶液浓度将有何影响?(填偏大、偏小、不变),没有进行A操作时浓度偏小;加蒸馏水时不慎超过了刻度线时浓度偏小;定容时俯视时浓度偏大.
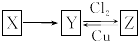 X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如图所示的转化关系(其他物质省略):
X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如图所示的转化关系(其他物质省略):