题目内容
下列表达式错误的是( )
A、甲基的电子式: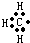 |
B、碳原子的价电子轨道表示式: |
| C、硫离子的核外电子排布式:1s22s22p6 |
| D、碳-14原子:614C |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.甲基中存在3个碳氢键,碳原子最外层为7个电子;
B.碳原子最外层为L层,2s、2p轨道各含有2个电子;
C.硫离子核外含有3个电子层,核外电子总数为18;
D.元素符号的左上角为质量数、左下角为质子数,质量数=质子数+中子数.
B.碳原子最外层为L层,2s、2p轨道各含有2个电子;
C.硫离子核外含有3个电子层,核外电子总数为18;
D.元素符号的左上角为质量数、左下角为质子数,质量数=质子数+中子数.
解答:
解:A.甲基中含有3个碳氢共用电子对,中心原子碳原子的最外层含有7个电子,甲基的电子式为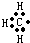 ,故A正确;
,故A正确;
B.碳原子价电子为2s、2p,各含有2个分子,碳原子的价电子轨道表示式为 ,故B正确;
,故B正确;
C.硫离子核外电子总数为18,核外含有3个电子层,硫离子的核外电子排布式为1s22s22p63s23p6,故C错误;
D.碳-14原子的核电荷数=质子数=6,质量数为14,该原子可以表示为614C,故D正确;
故选C.
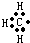 ,故A正确;
,故A正确;B.碳原子价电子为2s、2p,各含有2个分子,碳原子的价电子轨道表示式为
 ,故B正确;
,故B正确;C.硫离子核外电子总数为18,核外含有3个电子层,硫离子的核外电子排布式为1s22s22p63s23p6,故C错误;
D.碳-14原子的核电荷数=质子数=6,质量数为14,该原子可以表示为614C,故D正确;
故选C.
点评:本题考查了化学用语的表示方法判断,题目难度中等,注意掌握电子式、电子轨道表示式、元素符号等化学用语的表示方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O Cl2→Cl-MnO4-→Mn2+ HNO3→NO,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
| A、H2O2 |
| B、Cl2 |
| C、MnO4- |
| D、HNO3 |
下列各项中,理由、结论及因果关系均正确的是( )
| A、由于键能EN≡N>ECl-Cl,故单质的沸点:N2>Cl2 |
| B、由于分子中可电离的H+个数H2SO4>CH3COOH,故两者的酸性:H2SO4>CH3COOH |
| C、由于元素的非金属性N>P,故氢化物的稳定性:NH3>PH3 |
| D、由于金属性Fe>Cu,故还原性Fe2+>Cu |
下列有关说法正确的是( )
| A、煮沸饱和的FeCl3溶液能得到红褐色的氯化铁胶体 |
| B、根据化合物在水溶液或熔融状态下是否导电,将化合物分为电解质和非电解质 |
| C、能与碱反应生成盐和水的化合物称为酸性氧化物 |
| D、溶液与胶体的本质区别是能否发生丁达尔现象 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol NaHSO4晶体中离子总数为3NA |
| B、2.24 L 14CH4分子中所含中子数为0.8NA |
| C、0.1 L 3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| D、常温常压下,16gO2和O3混合气体含有NA个氧原子 |
在国际单位制中,物质的量的基本单位是( )
| A、千克 | B、摩尔 |
| C、立方米 | D、克/摩 |