题目内容
12.下列表示对应化学反应的离子方程式正确的是( )| A. | 钠和水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 碳酸钙与盐酸反应:CO32-+2Fe3+═Cu2++2Fe2+ | |
| C. | 铜片和氯化铁溶液反应:Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
分析 A.原子个数不守恒;
B.碳酸钙应保留化学式;
C.二者反应生成氯化亚铁和氯化铜;
D.不符合反应客观事实.
解答 解:A.钠和水反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.碳酸钙与盐酸反应:CaCO3+2H+═CO2↑+H2O+Ca2+,故B错误;
C.铜片和氯化铁溶液反应,离子方程式:Cu+2Fe3+═Cu2++2Fe2+,故C正确;
D.氯化铝溶液中加入过量氨水,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确离子反应实质是解题关键,注意离子方程式遵循原子个数守恒、遵循电荷守恒,遵循客观事实.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
3. 在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
 在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 反应温度:T1>T2 | B. | a、b两点的平衡常数:Kb>Ka | ||
| C. | a、c两点气体的颜色:a浅,c深 | D. | b、c两点的反应速率:v(b)>v(c) |
20.填上正确的除杂试剂和分离方法,来提纯下列物质(括号内为少量杂质).
| 序号 | 不纯物质 | 除杂试剂 | 分离方法 |
| ① | 苯(苯酚) | ||
| ② | 酒精(水) | ||
| ③ | 溴苯(Br2) | ||
| ④ | 乙烯(SO2) | ||
| ⑤ | 乙酸乙酯(乙酸) |
7.下列有关化学用语表示正确的是( )
| A. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | 氟原子的结构示意图: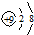 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同素异形体 | |
| D. | 碳酸钠的电离方程式:Na2CO3═Na2++CO32- |
17.用NA表示阿伏伽德罗常数的值,下列判断正确的是( )
| A. | 18H2O含有的氢原子数目为NA | |
| B. | 1molFe与足量盐酸反应失去的电子数为3NA | |
| C. | 标准状况下,22.4L等物质的量的CO2和O2混合气体中含有氧原子数为2NA | |
| D. | 2mol•L-1NaCl溶液中含有Na+个数为2NA |
4.在实验室,下列试剂中需要用棕色试剂瓶保存的是( )
| A. | 浓硝酸 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 浓氨水 |
1.与6.0g SO3所含的氧原子数相等的SO2的质量为( )
| A. | 3.6g | B. | 6.0g | C. | 7.2g | D. | 5.4g |
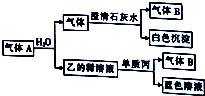 将一黑色固体单质甲投入乙的浓溶液中共热,剧烈反应产生混合气体A,A存在如图转化关系,试回答下列问题:
将一黑色固体单质甲投入乙的浓溶液中共热,剧烈反应产生混合气体A,A存在如图转化关系,试回答下列问题:

 +2H2O.
+2H2O.