题目内容
如图是锌、铜和稀硫酸形成的原电池,下列叙述不合理的是

A.溶液中H+向Zn电极移动
B.外电路中电流方向为:Cu→Zn
C.负极上的电极反应:Zn-2e-===Zn2+
D.有1 mol电子流过导线,则Cu电极上产生的H2为11.2 L(标准状况)
A
【解析】
试题分析:A、原电池中阳离子向正极移动,铜是正极,锌是负极,A错误;B、电池中电流是从正极流向负极,即该原电池中外电路中电流方向为:Cu→Zn,B正确;C、锌是负极失去电子,电极反应式为Zn-2e-=Zn2+,C正确;D、氢离子在正极得到电子,电极反应式为2H++2e-=H2↑,则有1 mol电子流过导线,则Cu电极上产生的H2物质的量是0.5mol,在标准状况下的体积为11.2 L,D正确,答案选A。
考点:考查铜锌原电池的有关判断

练习册系列答案
相关题目
 Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是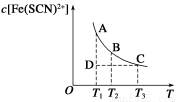
 2Z(g) ΔH<0,达到平衡时,下列说法正确的是
2Z(g) ΔH<0,达到平衡时,下列说法正确的是