题目内容
17.下列指定反应的离子方程式书写正确的是( )| A. | 少量SO2 通入漂白粉溶液中:SO2+H2O+Ca2++3C1O-═CaSO4↓+2HC1O+Cl- | |
| B. | 石灰水与过量小苏打溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | FeCl2溶液中通入 C12:Fe2++Cl2═Fe3++2Cl- | |
| D. | NaAlO2 溶液中通入过量CO2:AlO2-+4CO2+2H2O═A13++4HCO3- |
分析 A.发生氧化还原反应生成硫酸钙;
B.石灰水完全反应,生成碳酸钙、碳酸钠和水;
C.电子、电荷不守恒;
D.反应生成氢氧化铝和碳酸氢钠.
解答 解:A.少量SO2 通入漂白粉溶液中的离子反应为SO2+H2O+Ca2++3C1O-═CaSO4↓+2HC1O+Cl-,故A正确;
B.石灰水与过量小苏打溶液反应的离子反应为Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32-,故B错误;
C.FeCl2溶液中通入C12的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.NaAlO2 溶液中通入过量CO2的离子反应为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
7.在一定温度和压强下,把装有NO和NO2的混合气体的试管倒立于水中,充分反应后,试管内气体的体积缩小为原气体体积的$\frac{1}{2}$,则原混合气体中NO和NO2的体积比为( )
| A. | 3:l | B. | 1:3 | C. | 2:3 | D. | 3:2 |
8.常温下,取铝土矿(含有Al2O3、FeO、Fe2O3、SiO2等物质)用硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
| A. | 加入过量NaOH溶液:Na+、AlO2-、OH-、SO42- | |
| B. | 加入过量氨水:NH4+、Al3+、OH-、SO42- | |
| C. | 通入过量SO2:Fe2+、H+、SO32-、SO42- | |
| D. | 加入过量NaClO溶液:Fe2+、Na+、ClO-、SO42- |
5.从海带中提取碘应该包括灼烧、溶解、过滤、氧化、萃取、蒸馏等过程.下列有关图示操作正确的是( )
| A. | 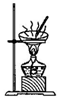 用装置甲将海带灼烧成灰 | B. | 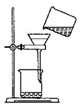 用装置乙过滤得含I-的溶液 | ||
| C. | 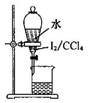 用装置丙分离出碘的CCl4溶液 | D. | 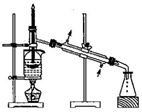 用装置丁蒸馏获得碘并回收CCl4 |
2.对反应A(s)+3B(g)?2C(g)+D(g)来说,下列反应速率最快的是( )
| A. | v(A)=0.02 mol/(L•s) | B. | v(B)=0.6 mol/(L•min) | ||
| C. | v(C)=0.5 mol/(L•min) | D. | v(D)=0.01 mol/(L•s) |
9.下列物质中,不属于合金的是( )
| A. | 青铜 | B. | 不锈钢 | C. | 硬铝 | D. | 黄金 |
6.某无色溶液中加入铝片后有氢气产生,则下列离子在该溶液中肯定能大量共存的是( )
| A. | Na+ | B. | Mg2+ | C. | CO32- | D. | MnO4- |
9.部分弱酸的电离平衡常数如下表:
(1)在温度相同时,各弱酸的Ka值与酸性的相对强弱的关系为Ka值越大,酸性越强.
(2)室温下①0.1mol•L-1 HCOONa,②0.1mol•L-1 NaClO,③0.1mol•L-1 Na2CO3,④0.1mol•L-1 NaHCO3溶液的pH由大到小的关系为③②④①.
(3)浓度均为0.1mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO2-3、CO32-、HSO3-、HCO3-浓度从大到小的顺序为SO32->CO32->HSO3->HCO3-.
(4)下列离子方程式正确的是bd(填字母).
a.2ClO-+H2O+CO2═2HClO+CO32- b.2HCOOH+CO32-═2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-═2HCOOH+SO32- d.Cl2+H2O+2CO32-═2HCO${\;}^{{\;}^{-}}$3+Cl-+ClO-
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(HCOO-)>c(Na+)>c(H+)>c(OH-).
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)室温下①0.1mol•L-1 HCOONa,②0.1mol•L-1 NaClO,③0.1mol•L-1 Na2CO3,④0.1mol•L-1 NaHCO3溶液的pH由大到小的关系为③②④①.
(3)浓度均为0.1mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO2-3、CO32-、HSO3-、HCO3-浓度从大到小的顺序为SO32->CO32->HSO3->HCO3-.
(4)下列离子方程式正确的是bd(填字母).
a.2ClO-+H2O+CO2═2HClO+CO32- b.2HCOOH+CO32-═2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-═2HCOOH+SO32- d.Cl2+H2O+2CO32-═2HCO${\;}^{{\;}^{-}}$3+Cl-+ClO-
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(HCOO-)>c(Na+)>c(H+)>c(OH-).
 完成下列题目
完成下列题目