题目内容
13.甲、乙是由同主族元素R、Z组成的两种单质,常温下能进行如下反应:甲+乙+H2O--HRO3+HZ(未配平).下列说法不正确的是( )| A. | R原子最外层电子数为5 | B. | 单质的氧化性:甲<乙 | ||
| C. | 原子半径:R>Z | D. | HRO3与HZ计量数之比为1:5 |
分析 甲、乙是由同主族元素R、Z组成的两种单质,常温下能进行如下反应:甲+乙+H2O→HRO3+HZ(未配平),反应中Z表现-1价,最外层电子数为7,则R、Z处于ⅦA族,R表现+5价,非金属性Z>R,单质氧化性与非金属性一致,同主族自上而下原子半径增大,结合电子转移守恒计算HRO3与HZ的化学计量数之比.
解答 解:甲、乙是由同主族元素R、Z组成的两种单质,常温下能进行如下反应:甲+乙+H2O→HRO3+HZ(未配平),反应中Z表现-1价,最外层电子数为7,则R、Z处于ⅦA族,R表现+5价,非金属性Z>R,
A.R原子最外层电子数为7,故A错误;
B.无法确定甲乙的元素组成,则无法判断其氧化性强弱,故B错误;
C.非金属性Z>R,则原子序数Z<R,同主族自上而下原子半径增大,故原子半径:R>Z,故C正确;
D.根据电子转移守恒5n(HRO3)=n(HZ),故HRO3与HZ的化学计量数之比为1:5,故D正确,
故选AB.
点评 本题考查结构性质位置关系综合应用,题目难度中等,根据Z的氢化物化合价确定所处主族为解答关键,注意掌握元素周期律内容、元素周期表结构,试题培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.一个集气瓶中放有一团棉花,向其中倒入CO2气体时棉花燃烧起来,则棉花中可能包有( )
| A. | 烧碱 | B. | 氧化钠 | C. | 过氧化钠 | D. | 小苏打 |
4.(1)某学生为了探究铝与盐酸反应过程中的速率变化,他用排水集气法收集反应放出的氢气,实验记录如下:
①哪一时间段(即0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3min,原因是因该反应是放热反应,此时温度高.
②哪一段时段的反应速率最小4~5 min,原因是此时H+浓度小.
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气的体积,他事先在盐酸中加入等体积的下列溶液:A、蒸馏水 B、CuCl2溶液 C、NaNO3溶液,以减慢反应速率,你认为可行的是A,不可行的是BC,不可行的理由是加入少量CuCl2晶体时,CuCl2会与锌反应置换出铜,Al、铜与酸会形成原电池,发生原电池反应而加快反应速率;加入硝酸钠溶液时,存在的硝酸根离子和氢离子相当于存在硝酸,金属铝和硝酸反应不会产生氢气..
(3)下列各分子中,所有原子都满足最外层为8电子结构的是③④⑥⑦
①H2O ②BF3 ③CCl4 ④PCl3 ⑤SO3 ⑥N2 ⑦CO2.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 150 | 300 | 380 | 410 |
②哪一段时段的反应速率最小4~5 min,原因是此时H+浓度小.
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气的体积,他事先在盐酸中加入等体积的下列溶液:A、蒸馏水 B、CuCl2溶液 C、NaNO3溶液,以减慢反应速率,你认为可行的是A,不可行的是BC,不可行的理由是加入少量CuCl2晶体时,CuCl2会与锌反应置换出铜,Al、铜与酸会形成原电池,发生原电池反应而加快反应速率;加入硝酸钠溶液时,存在的硝酸根离子和氢离子相当于存在硝酸,金属铝和硝酸反应不会产生氢气..
(3)下列各分子中,所有原子都满足最外层为8电子结构的是③④⑥⑦
①H2O ②BF3 ③CCl4 ④PCl3 ⑤SO3 ⑥N2 ⑦CO2.
1.化学与生产和生活密切相关,下列说法正确的是( )
| A. | 聚乙烯塑料的老化是因为发生了加成反应 | |
| B. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| C. | 棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 | |
| D. | 在清洗地板时,84消毒液和洁厕灵(主要成分是盐酸)不能混合使用 |
18.硫酸镁在药疗上常用作导泻剂.硫酸镁(MgSO4)属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
2.下列实验方法或操作正确的是( )
| A. | 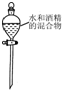 分离水和酒精 | |
| B. |  蒸发NH4Cl溶液得到NH4Cl晶体 | |
| C. | 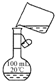 配制一定物质的量浓度溶液时转移溶液 | |
| D. |  除去氯气中的氯化氢 |
3.取少量无机盐溶液试样对其中的离子进行检验.下列判断正确的是( )
| A. | 加入盐酸,产生白色沉淀,则试样中一定有Ag+ | |
| B. | 加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-或HCO3- | |
| C. | 加入NaOH溶液微热,产生使湿润红色石蕊试纸变蓝气体,则试样中一定有NH4+ | |
| D. | 加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,则试样中一定有SO42- |
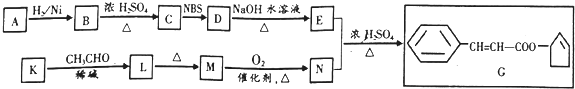
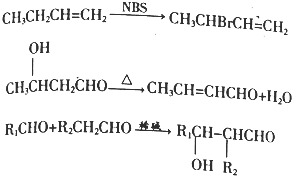
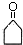
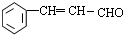 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2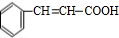
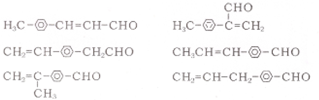 任意一种.
任意一种.