题目内容
下列实验设计方案中,可行的是( )
| A、用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 |
| B、在某试样中加入NaOH溶液加热,产生能使蓝色石蕊试纸变红的气体即证明有NH4+ |
| C、焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.CO2和HCl气体均能与NaOH溶液反应;
B.根据氨气水溶液呈碱性的性质判断;
C.应用盐酸清洗;
D.从防止液体重新混合而污染的角度分析.
B.根据氨气水溶液呈碱性的性质判断;
C.应用盐酸清洗;
D.从防止液体重新混合而污染的角度分析.
解答:
解:A.CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,故A错误;
B.氨气水溶液呈碱性,可使红色石蕊试纸变蓝,故B错误;
C.硫酸盐难以挥发,应用盐酸清洗铁丝,故C错误;
D.下层液体从下口放出,上层液体从上口倒出的目的是防止液体重新混合而污染,操作正确,故D正确.
故选D.
B.氨气水溶液呈碱性,可使红色石蕊试纸变蓝,故B错误;
C.硫酸盐难以挥发,应用盐酸清洗铁丝,故C错误;
D.下层液体从下口放出,上层液体从上口倒出的目的是防止液体重新混合而污染,操作正确,故D正确.
故选D.
点评:本题考查化学实验方案的评价,题目难度中等,本题易错点为C,注意焰色反应实验的方法.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列实验方案正确且能达到相应实验预期目的是( )
A、 制取少量蒸馏水 |
B、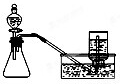 用铜和浓硝酸混合制取少量NO2 |
C、 比较MnO2、Cl2、I2的氧化性 |
D、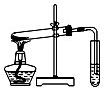 探究NaHCO3的热稳定性 |
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0g,若上述气体为NO和NO2的混合物,且体积比为1:1,则v可能为( )
| A、9.0L | B、13.5L |
| C、10.7L | D、16.8L |
用已知浓度的盐酸来测定某Na2CO3溶液的浓度,若配制Na2CO3溶液时所用的Na2CO3中分别含有①NaOH,②NaCl,③NaHCO3,④K2CO3杂质时,所测结果偏低的是( )
| A、① | B、② | C、②③ | D、②③④ |
阿司匹林是日常生活中应用广泛的医药之一.它可由下列方法合成下列说法正确的是( )

| A、与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物共有3种 |
| B、用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① |
| C、反应②中加入过量的NaHCO3有利提高阿司匹林的产率 |
| D、1mol阿司匹林最多可以和2molNaOH反应 |
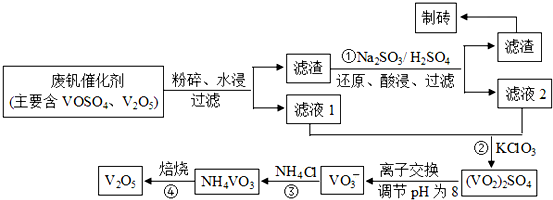
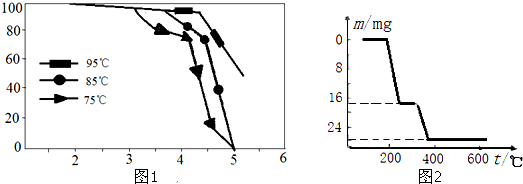
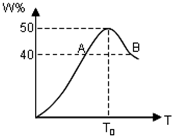 2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线:
2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线: