题目内容
11.下列有关NO、NO2、SO2的说法正确的是( )| A. | 它们都能与水反应生成对应的酸 | |
| B. | 标准状况下它们都是无色无味的气体 | |
| C. | 分子中氧元素的质量分数:NO>NO2>SO2 | |
| D. | 实验室可以利用氧化还原反应分别制备NO、NO2、SO2 |
分析 A、一氧化氮不溶于水也不与水反应;
B、二氧化氮是红棕色的气体,二氧化硫有刺激性气味;
C、二氧化氮分子中二个氧原子,而一氧化氮只有一个氧原子;
D、实验室制备NO用铜与稀硝酸发生氧化还原反应、NO2用铜与浓硝酸发生氧化还原反应、SO2用铜与浓硫酸在加热条件下发生氧化还原反应.
解答 解:A、一氧化氮不溶于水也不与水反应,二氧化氮与水反应生成硝酸,二氧化硫与水反应生成亚硫酸,故A错误;
B、二氧化氮是红棕色的气体,二氧化硫有刺激性气味,故B错误;
C、二氧化氮分子中二个氧原子,而一氧化氮只有一个氧原子,所以分子中氧元素的质量分数:NO<NO2,故C错误;
D、实验室制备NO用铜与稀硝酸发生氧化还原反应、NO2用铜与浓硝酸发生氧化还原反应、SO2用铜与浓硫酸在加热条件下发生氧化还原反应,所以三种气体都可用氧化还原反应制取,故D正确;
故选D.
点评 本题考查NO、NO2、SO2的物理和化学性质和分子的组成以及各自的制法,综合性强,但比较容易.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
1.下列盛放试剂的方法,错误的是( )
| A. | 氢氟酸盛放在玻璃试剂瓶中 | |
| B. | 浓硝酸盛在棕色试剂瓶中 | |
| C. | 氢氧化钠溶液盛在带橡皮塞的玻璃瓶中 | |
| D. | 氯水盛在棕色试剂瓶中,并放置在冷暗处 |
2. 如图试管中盛有酸雨浸泡过的铁钉,U形管中盛有一段红墨水.开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升.下列说法不正确的是( )
如图试管中盛有酸雨浸泡过的铁钉,U形管中盛有一段红墨水.开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升.下列说法不正确的是( )
 如图试管中盛有酸雨浸泡过的铁钉,U形管中盛有一段红墨水.开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升.下列说法不正确的是( )
如图试管中盛有酸雨浸泡过的铁钉,U形管中盛有一段红墨水.开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升.下列说法不正确的是( )| A. | 开始时发生的是析氢腐蚀 | B. | -段时间后发生的是吸氧腐蚀 | ||
| C. | 两段时间内负极的电极反应相同 | D. | 两段时间内正极的电极反应相同 |
6.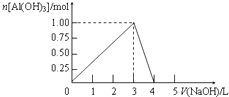 向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果正确的是( )
向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果正确的是( )
 向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果正确的是( )
向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果正确的是( )| A. | 反应过程中,沉淀最多时的质量为7.8g | |
| B. | AlCl3溶液的浓度为2.0 mol•L-1 | |
| C. | 得到39g沉淀时,消耗的NaOH溶液体积为1.5L或3.5L | |
| D. | 当V(NaOH)=4L时,得到的溶液中Na+、Cl-浓度相等 |
16.下列关于等质量的14CO2与N218O说法不正确的是( )
| A. | 分子数之比为1:1 | B. | 原子数之比为1:1 | C. | 中子数之比为1:1 | D. | 密度之比为1:1 |
3.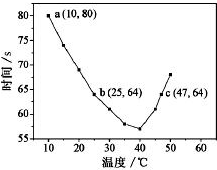 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )| A. | 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 | |
| B. | 当NaHSO3完全消耗时的离子方程式为:6HSO3-+2IO3-=6SO42-+2I-+6H+ | |
| C. | 图中a点对应的NaHSO3反应速率为5.5×10-5mol•L-1•s-1 | |
| D. | 温度高于40℃时,淀粉不宜用作该实验的指示剂 |
 金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得判迅猛发展.
金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得判迅猛发展.