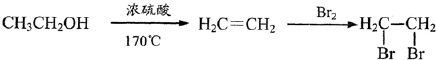题目内容
下列关于反应能量的说法正确的是( )
| A、Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s);△H=-216kJ?mol-1,反应物总能量>生成物总能量 |
| B、相同条件下,如果1mol氢原子所具有的能量为E1,1mol氢分子的能量为E2.则2E1>E2 |
| C、l0lkPa 时,2H2(g)+O2(g)=2H2O(1);△H=-571.6kJ?mol-1,H2的燃烧热为571.6kJ/mol |
| D、H+ (aq)+OH-(aq)=H2O(l);△H=-57.3kJ?mol-1,含 1molNaOH 的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3kJ的热量 |
考点:有关反应热的计算,化学反应的能量变化规律,燃烧热
专题:
分析:A、反应是放热反应,依据能量守恒分析;
B、原子能量高于分子能量,形成化学键放出能量;
C、燃烧热必须是1mol物质燃烧生成最稳定的化合物所放出的能量;
D、中和热是强酸和强碱发生中和反应生成1mol水时,所放出的热量.
B、原子能量高于分子能量,形成化学键放出能量;
C、燃烧热必须是1mol物质燃烧生成最稳定的化合物所放出的能量;
D、中和热是强酸和强碱发生中和反应生成1mol水时,所放出的热量.
解答:
解:A、Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)△H=-216 kJ/mol,反应放热,反应物总能量大于生成物总能量,故A正确;
B、原子能量高于分子能量,形成化学键放出能量,相同条件下,如果1mol氢原子所具有的能量为E1,1mol氢分子所具有的能量为E2,则2E1>E2,故B正确;
C、H2的燃烧热必须是1mol物质燃烧生成最稳定的化合物液态水时所放出的能量,该选项中表示2mol氢气燃烧放出571.6 kJ热量,故C错误;
D、中和热是强酸和强碱发生中和反应生成1mol水时,所放出的热量,1molNaOH的氢氧化钠溶液与含0.5molH2SO4的浓硫酸混合时,浓硫酸溶于水放热,所以导致△H<-57.3kJ?mol-1,故D错误;
故选AB.
B、原子能量高于分子能量,形成化学键放出能量,相同条件下,如果1mol氢原子所具有的能量为E1,1mol氢分子所具有的能量为E2,则2E1>E2,故B正确;
C、H2的燃烧热必须是1mol物质燃烧生成最稳定的化合物液态水时所放出的能量,该选项中表示2mol氢气燃烧放出571.6 kJ热量,故C错误;
D、中和热是强酸和强碱发生中和反应生成1mol水时,所放出的热量,1molNaOH的氢氧化钠溶液与含0.5molH2SO4的浓硫酸混合时,浓硫酸溶于水放热,所以导致△H<-57.3kJ?mol-1,故D错误;
故选AB.
点评:本题考查化学反应中的能量变化的有关知识,主要是反应的能量守恒的应用,掌握放热反应,燃烧热、中和热的概念是解答的关键,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列元素属于卤族元素的是( )
| A、Cl | B、P | C、He | D、Li |
盐酸、醋酸和碳酸氢钠是生活中常见的物质,下列表述正确的是( )
| A、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B、将pH相同的盐酸和醋酸稀释相同倍数,醋酸的pH变化大 |
| C、10 mL0.10 mol?L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、中和体积与pH都相同HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同 |
可逆反应mA(s)+nB(g)?eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数w(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示.下列叙述正确的是( )
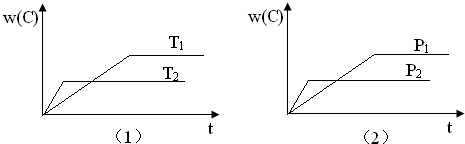

| A、达到平衡后,若使用催化剂,C的体积分数将增大 |
| B、当平衡后,若温度升高,化学平衡向逆反应方向移动 |
| C、化学方程式中,n>e+f |
| D、达到平衡后,增加A的质量有利于化学平衡向正反应方向移动 |
PCl5(气)?PCl3(气)+Cl2(气)△H>0 当反应达到平衡时,下列措施:①降温 ②恒容通入惰性气体 ③增加Cl2的浓度 ④加压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高PCl5质量分数的是( )
| A、①②④ | B、①③④ |
| C、②③⑥ | D、③⑤⑥ |
下列说法正确的是( )
| A、在相同条件下,若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | ||
| B、由“C(石墨)=C(金刚石);△H=+119kJ?mol-1”可知,金刚石比石墨稳定 | ||
| C、在稀溶液中:H+(aq)+OH q)=H2O(l);△H=-57.3l kJ?mol-1,若将含0.5mol H2SO4的浓硫酸与lmol NaOH溶液混合,放出的热量大于57.31 kJ | ||
D、在101KPa时,2g H2生成液态水,放出285.8 kJ 热量,氢气燃烧的热化学方程式表示为:H2(g)+
|
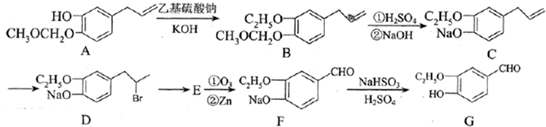
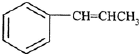 为原料制备
为原料制备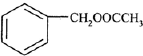 的合成路线流程图(无机试剂
的合成路线流程图(无机试剂