题目内容
下列两种物质中含有的氧原子数不同的是( )
| A、质量比为2:1的SO2和O2 |
| B、9g水和22gCO2 |
| C、12gNO和9.8gH2SO4 |
| D、物质的量相同的H2SO4和H3PO4 |
考点:物质的量的相关计算
专题:
分析:根据n=
计算各物质的量,结合分子含有氧原子数目计算氧原子物质的量,据此判断.
| m |
| M |
解答:
解:A.根据n=
可知,质量比为2:1的SO2和O2的物质的量之比为
:
=1:1,二者分子均含有2个氧原子,故含有氧原子数目相等,故A不选;
B.9g水的物质的量为
=0.5mol,含有0.5mol,22gCO2的物质的量为
=0.5mol,含有氧原子为0.5mol×2=1mol,二者含有氧原子数目不相等,故B选;
C.12gNO的物质的量为
=0.4mol,含有0.4mol氧原子,9.8gH2SO4的物质的量为
=0.1mol,含有氧原子为0.1mol×4=0.4mol,二者含有氧原子数目相等,故B不选;
D.H2SO4和H3PO4分子均含有4个氧原子,物质的量相等的H2SO4和H3PO4含有氧原子数目相等,故D不选,
故选B.
| m |
| M |
| 2 |
| 64 |
| 1 |
| 32 |
B.9g水的物质的量为
| 9g |
| 18g/mol |
| 22g |
| 44g/mol |
C.12gNO的物质的量为
| 12g |
| 30g/mol |
| 9.8g |
| 98g/mol |
D.H2SO4和H3PO4分子均含有4个氧原子,物质的量相等的H2SO4和H3PO4含有氧原子数目相等,故D不选,
故选B.
点评:本题考查物质的量有关计算,侧重微粒数目计算,有利于基础知识的巩固.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
聚丙烯酸钠(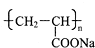 )具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )
)具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )
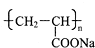 )具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )
)具有超强吸水性,能吸收空气中的水分,可用于矿山道路运输抑尘等.下列叙述不正确的是( )| A、聚丙烯酸钠属于混合物 |
| B、聚丙烯酸钠属于天然有机高分子化合物 |
| C、聚丙烯酸钠可用于生产“尿不湿” |
| D、路面喷洒聚丙烯酸钠溶液能抑制扬尘,一定程度上能预防雾霾和PM2.5 |
在《化学1》P.44的【拓展视野】中介绍了二氧化氯是一种新型灭菌消毒剂.以下反应可制得ClO2:2NaClO3+Na2SO3+H2SO4?2ClO2+2Na2SO4+H2O.对于该反应,下列说法中正确的是( )
| A、该反应是复分解反应 |
| B、Na2SO3发生氧化反应 |
| C、H2SO4是氧化剂 |
| D、NaClO3是还原剂 |
下列说法正确的是( )
| A、还原剂失去电子变成还原产物 |
| B、氧化剂被氧化成还原产物 |
| C、氧化剂是得到电子,发生还原反应的物质 |
| D、还原剂是化合价下降得到电子被氧化的物质 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、常温常压下,28 g氮气所含的原子数为2NA |
| B、22.4 L甲烷(CH4)所含的原子数为5NA |
| C、0.5 molCuO的摩尔质量为40g/mol |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3NA |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、46g NO2气体中含有的分子数一定为NA |
| B、1molCH3+(碳正离子)中含有电子数为10NA |
| C、1mol铜与足量硫蒸气反应,转移电子数为2NA |
| D、1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2NA个电子 |
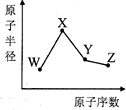 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子数变化如图所示.已知W的一种核素的质量数为18,中子数为10,X和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子数变化如图所示.已知W的一种核素的质量数为18,中子数为10,X和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法正确的是( )| A、对应简单离子半径:X>W |
| B、对应气态氢化物的稳定性Y>Z |
| C、化合物XZW既含离子键,又含共价键 |
| D、Y的氧化物与Z的氧化物和X的最高价氧化物对应的水化物均能反应 |