题目内容
已知四种盐的溶解度(S)曲线如右图所示,下列说法不正确的是
| A.将MgCl2溶液蒸干后不可能得到MgCl2固体 |
| B.将NaCl溶液蒸干可得NaOH固体 |
| C.NaClO3中混有少量NaCl杂质,可用重结晶法提纯 |
| D.可用MgCl2和NaClO3制备Mg(ClO3)2 |
B
解析试题分析:因MgCl2能够水解,水解产生了Mg(OH)2和HCl,加热水解平衡正向移动,氯化氢易挥发,所以将MgCl2溶液蒸干可得固体为Mg(OH)2,故A错误;因NaCl不会发生水解,所以将NaCl溶液蒸干可得NaCl固体,,故B错误;NaClO3与NaCl的溶解度随温度变化差别较大,所以可以可用重结晶法提纯,故C正确;反应MgCl2+2NaClO3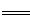 Mg(ClO3)2+2NaCl类似于侯德榜制碱法生成NaHCO3的原理,因为NaCl溶解度小而从溶液中析出,使反应向生成Mg(ClO3)2的方向进行,故D正确;
Mg(ClO3)2+2NaCl类似于侯德榜制碱法生成NaHCO3的原理,因为NaCl溶解度小而从溶液中析出,使反应向生成Mg(ClO3)2的方向进行,故D正确;
考点:考查溶解度曲线的意义及应用。

练习册系列答案
相关题目
下列实验设计能够成功的是( )
| | 实验目的 | 实 验 步 骤 及 现 象 |
| A | 检验亚硫酸钠试 样是否变质 |  |
| B | 检验某盐是否为铵盐 |  |
| C | 证明酸性条件 H2O2氧化性比I2强 |  |
| D | 除去氯化钠晶体中少量硝酸钾 |  |
下列实验方法正确且能达到目的的是
| A.用装置I除去CO2中的SO2 | B.实验室用装置II制备NH3 |
| C.用装置III制备乙烯 | D.装置IV比较酸性H2CO3>苯酚 |
下列四组实验,根据实验事实得出的结论,正确的是
| A.在某试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解——原未知试液中一定含有SO42- |
| B.在某未知试液中加入浓的NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体——原未知试液中一定含有NH4+ |
| C.在某未知试液中滴加盐酸产生无色气体,将该气体通入足量澄清石灰水中得白色沉淀——原未知试液中一定含有CO32- |
| D.用洁净的铂丝蘸取未知物质,放在无色火焰上灼烧,其焰色为黄色——该未知物中一定只含钠元素 |
只用一种试剂就能鉴别出NH4Cl、Na2SO4、(NH4)2CO3三种溶液,应选用下列试剂中的
| A.BaCl2 | B.HCl | C.NaOH | D.Ba(OH)2 |
用下列实验装置进行相应实验,能达到实验目的的是( )。
| A.用图1所示装置除去Cl2中含有的少量HCl |
| B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3所示装置制取少量纯净的CO2气体 |
| D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
下列有关实验原理、方法、操作或结论不正确的是( )
| A.除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
| B.用水湿润pH试纸测量某溶液的pH,一定会产生实验误差 |
| C.容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,必须用所盛溶液润洗几次后方可使用 |
| D.称取a克Na2CO3和NaHCO3混合物充分加热,减重b克,可测定混合物中Na2CO3的质量分数 |
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )。
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 某气体遇湿润的淀粉碘化钾试纸 | 试纸变蓝 | 该物质一定是氯气 |
| B | 滴加氯水和苯,振荡、静置 | 上层溶液显紫色 | 原溶液中有I- |
| C | 用洁净铂丝蘸取少量溶液进行焰色反应 | 火焰呈黄色 | 原溶液一定是钠盐溶液 |
| D | 滴加BaCl2溶液 | 产生不溶于稀硝酸的白色沉淀 | 原溶液一定含有Ag+ |