题目内容
14.某温度下,BaSO4与水组成的混合物中,存在如下过程:BaSO4(s)?Ba2+(aq)+SO42-(aq),向其中加入少量Na2SO4固体,下列说法错误的是( )| A. | BaSO4溶解的量减小 | B. | BaSO4的电离程度减小 | ||
| C. | 溶液的导电能力增大 | D. | c (Ba2+)与c (SO42-)的乘积增大 |
分析 向其中加入少量硫酸钠固体,硫酸根离子浓度增大,平衡向着逆向移动,则硫酸钡的溶解度减小;硫酸钡为强电解质,在溶液中完全电离,则其电离程度不变;由于温度不变,则难溶物溶度积不变,故c(Ba2+)与c(SO42-)的乘积不变;溶液中离子浓度增大,溶液的导电性会增强,据此进行解答.
解答 解:A.加入硫酸钠后,溶液中硫酸根离子浓度增大,溶解平衡向着逆向移动,导致硫酸钡的溶解的量减小,故A正确;
B.硫酸钡在溶液中完全电离,则加入硫酸钠后,硫酸钡的电离程度不变,仍然为100%,故B错误;
C.加入硫酸钠后,溶液中离子浓度增大,则溶液的导电性增强,故C正确;
D.c(Ba2+)与c(SO42-)的乘积为溶度积,由于温度不变,则硫酸钡的溶度积不变,故D错误;
故选BD.
点评 本题考查了难溶物溶解平衡及其影响,题目难度中等,明确影响溶解平衡的因素为解答关键,注意溶度积只与难溶物性质、温度有关,为易错点,试题培养了学生的灵活应用能力.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
15.下列化学用语正确的是( )
| A. | 甲基的电子式: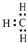 | B. | 氮原子的电子排布图: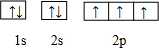 | ||
| C. | 淀粉的实验式:CH2O | D. | 聚乙炔结构简式: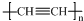 |
5.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)?A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡.下列说法中正确的是( )
| A. | 反应速率:乙>甲 | B. | 平衡时C的体积分数:乙>甲 | ||
| C. | 平衡时C的转化率:乙>甲 | D. | 平衡时A的物质的量:甲>乙 |
2.某溶液中含有HCO3-、SO32-、CO32-、CH3COO-4种阴离子.向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)( )
| A. | CH3COO- | B. | SO32- | C. | CO32- | D. | HCO3- |
9.在密闭容器中盛有H2、O2、Cl2三种气体,电火花点燃后,三种气体都正好反应完全,冷却到室温,所得溶液的质量分数为25.26%,则原混合气体中三者的分子个数之比为( )
| A. | 15:8:1 | B. | 13:6:1 | C. | 9:6:1 | D. | 6:3:1 |
19.在分子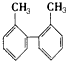 中,在同一平面内的碳原子最少应有( )
中,在同一平面内的碳原子最少应有( )
 中,在同一平面内的碳原子最少应有( )
中,在同一平面内的碳原子最少应有( )| A. | 7个 | B. | 8个 | C. | 9个 | D. | 14个 |
6.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol苯分子中含有C═C键的数目为3NA | |
| B. | 含1molNa2CO3的溶液中,阴离子总数大于NA | |
| C. | 1molFeI2与足量氯气反应时转移的电子数为2NA | |
| D. | 标准状况下,22.4L空气中含有的氧原子数为2NA |
3.使用SNCR脱硝技术的主反应为:
4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g);△H
4N2(g)+6H2O(g);△H
副反应及773K时平衡常数如表所示
(1)主反应△H=-1632.5kJ•mol-1,773K时主反应平衡常数K=4.6×1043L•mol-1
(2)图2表示在密闭体系中进行实验,起始投入一定量NH3、NO、O2,测定不同温度下,在相同时间内各组分的浓度.
①图中a、b、c三点,主反应速率最大的是c
②试解释N2浓度曲线先上升后下降的原因先上升:反应还未到达平衡状态,温度越高,化学反应速率越快,单位时间内N2浓度越大;后下降:达到平衡状态后,随着温度升高,因反应正向放热,平衡逆向移动,且随温度升高有副产物的生成,N2浓度降低.
③550K时,欲提高N2O的百分含量,应采取的措施是采用合适的催化剂
(3)电化学催化净化NO是一种最新脱硝方法.原理示意图如图1,固体电解质起到传导O2-的作
用.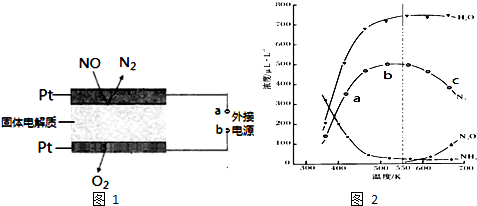
A为外接电源的负极(填“正”、“负”).通入NO的电极反应式为2NO+4e-=N2+2O2-.
4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g);△H
4N2(g)+6H2O(g);△H副反应及773K时平衡常数如表所示
| 反应 | △H(kJ•mol-1) | 平衡常数(K) |
| 4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g) | -905.5 | 1.1×1026mol•L-1 |
| 4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g) | -1104.9 | 4.4×1028 |
| 4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g) | -1269.0 | 7.1×1034L•mol-1 |
(2)图2表示在密闭体系中进行实验,起始投入一定量NH3、NO、O2,测定不同温度下,在相同时间内各组分的浓度.
①图中a、b、c三点,主反应速率最大的是c
②试解释N2浓度曲线先上升后下降的原因先上升:反应还未到达平衡状态,温度越高,化学反应速率越快,单位时间内N2浓度越大;后下降:达到平衡状态后,随着温度升高,因反应正向放热,平衡逆向移动,且随温度升高有副产物的生成,N2浓度降低.
③550K时,欲提高N2O的百分含量,应采取的措施是采用合适的催化剂
(3)电化学催化净化NO是一种最新脱硝方法.原理示意图如图1,固体电解质起到传导O2-的作
用.

A为外接电源的负极(填“正”、“负”).通入NO的电极反应式为2NO+4e-=N2+2O2-.
4.如图,反应2X(g)+Y(g)?2Z(g)△H<0,下列分析不正确的是( )
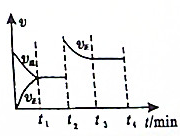

| A. | t2可能是升高温度 | |
| B. | t1时刻Y的体积分数可能比t3时刻Y的体积分数小 | |
| C. | t1时刻X的浓度可能比t3时刻X的浓度大 | |
| D. | t1时的平衡是从逆反应方向建立 |