题目内容
下列说法正确的是( )
| A、Li是最活泼的金属,F是最活泼的非金属 |
| B、Mg(OH)2碱性比Ca(OH)2强 |
| C、元素周期表中有7个主族,7个副族,1个0族,1个第Ⅷ族,共16纵行 |
| D、X2+的核外电子数目为18,则X在第四周期第ⅡA族 |
考点:碱金属的性质,元素周期表的结构及其应用
专题:
分析:A.同主族从上到下金属的活泼性依次增强,同周期从左到右非金属的活泼性增强;
B.同主族从上到下金属的活泼性依次增强,最高价氧化物碱性依次增强;
C.Ⅷ族占3个纵行;
D.阳离子:质子数=核外电子数+带电荷数.
B.同主族从上到下金属的活泼性依次增强,最高价氧化物碱性依次增强;
C.Ⅷ族占3个纵行;
D.阳离子:质子数=核外电子数+带电荷数.
解答:
解:A.最活泼的金属是Cs,最活泼的非金属是F,故A错误;
B.同主族从上到下元素的最高价氧化物对应水化物的碱的碱性逐渐增强,所以Mg(OH)2碱性比Ca(OH)2弱,故B错误;
C.元素周期表共有18纵行其中7个主族,7个副族,1个0族,1个Ⅷ族,一个Ⅷ族占三个纵行,故C错误;
D.X2+的核外电子数目为18,依据阳离子:质子数=核外电子数+带电荷数,所以X原子的质子数=18+2=20,为钙元素,在第四周期第ⅡA族,故D正确;
故选:D.
B.同主族从上到下元素的最高价氧化物对应水化物的碱的碱性逐渐增强,所以Mg(OH)2碱性比Ca(OH)2弱,故B错误;
C.元素周期表共有18纵行其中7个主族,7个副族,1个0族,1个Ⅷ族,一个Ⅷ族占三个纵行,故C错误;
D.X2+的核外电子数目为18,依据阳离子:质子数=核外电子数+带电荷数,所以X原子的质子数=18+2=20,为钙元素,在第四周期第ⅡA族,故D正确;
故选:D.
点评:本题考查了元素性质递变规律和元素周期表结构,明确元素周期表排布规律和元素周期律是解题关键,题目难度不大.

练习册系列答案
相关题目
实验是化学研究的基础.下列对实验现象的描述错误的是( )
 |  | 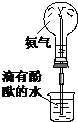 |  |
| ① | ② | ③ | ④ |
| A、实验①中溶液变黄色 |
| B、实验②试管中混合溶液变红色 |
| C、实验③中烧瓶内溶液变红色 |
| D、实验④中出现砖红色沉淀 |
将铁屑溶于过量盐酸后,再加入下列物质:①硫酸②硝酸锌③氯化铜④氯水,产生的Fe3+是( )
| A、①④ | B、②④ | C、只有④ | D、①③ |
相同质量的钠在下列情况下产生氢气最多的是( )
| A、投入到足量水中 |
| B、投入到足量盐酸中 |
| C、投入到足量CuSO4溶液中 |
| D、用刺有小孔的铝箔包好放入足量水中 |
下列有关物质与其用途(括号内为其用途)不相对应的是( )
| A、SiO2(制光纤) |
| B、氮化硅陶瓷(制导热剂) |
| C、钢化玻璃(汽车窗玻璃) |
| D、Si和Ge(半导体材料) |
下列关于电解质的说法正确的是( )
| A、不是电解质的物质就是非电解质 |
| B、将纯水加热至较高温度,Kw变大 |
| C、BaSO4不溶于水,其水溶液的导电能力很弱,所以为弱电解质 |
| D、电解质在任何状态下都能导电 |
根据下列反应,判断氧化性强弱正确的是( )
①2H2S+O2═2S↓+2H2O ②4NaI+O2+2H2O═4NaOH+2I2 ③Na2S+I2═2NaI+S↓
①2H2S+O2═2S↓+2H2O ②4NaI+O2+2H2O═4NaOH+2I2 ③Na2S+I2═2NaI+S↓
| A、O2>I2>S |
| B、O2>S>I2 |
| C、I2>O2>S |
| D、S>I2>O2 |
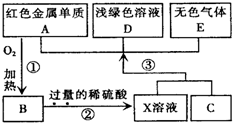 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答: