题目内容
9.在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+,下列说法不正确的是( )| A. | 可以利用该反应检验Mn2+ | |
| B. | 配平后的系数为2、5、8、2、10、16 | |
| C. | 该反应中酸性介质不能为盐酸 | |
| D. | 若有0.1mol还原产物生成,则转移电子0.5mol |
分析 2Mn2++5S2O82-+8X=2MnO42-+10SO42-+16H+中,Mn元素的化合价升高,S元素的化合价降低,由电荷守恒可知,X为中性物质,结合原子守恒可知X为H2O,以此来解答.
解答 解:A、由于MnO4-在溶液中显紫红色,所以可以利用该反应检验Mn2+,故A正确;
B、根据方程式可知,Mn元素的化合价从+2价升高到+7价,失去5个电子;S元素的化合价从+7价降低到+6价,得到1个电子,所以根据电子的得失守恒可知,故B正确;
C、酸性高锰酸钾溶液能氧化盐酸,生成氯气,所以该反应的介质不能用盐酸,故C正确;
D、由反应可知,反应中Mn元素化合价由+2价升高到+7价,变化5价,则有0.1mol氧化产物生成,则转移0.5mol电子,故D错误;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,选项B为解答的难点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.常温下,关于浓度相等的氢氧化钠和氨水,下列说法正确的是( )
| A. | NH3•H2O溶液的c(OH-)<NaOH溶液的c(OH-) | |
| B. | c(Na+)=c(NH4+) | |
| C. | 等体积的氢氧化钠和氨水溶液与足量盐酸完全反应,NaOH消耗的盐酸体积多 | |
| D. | 将等体积的氢氧化钠和氨水溶液加水稀释相同倍数,NaOH溶液的pH大 |
20.铝灰的回收利用方法很多,现用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O,工艺流程如下:
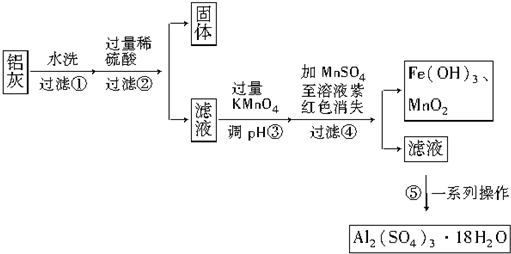
请回答下列问题:
(1)加入过量稀硫酸溶解Al2O3的离子方程式是6H++Al2O3═2Al3++3H2O.
(2)流程中加入的KMnO4也可用H2O2代替,若用H2O2发生反应的化学方程式为H2O2+2FeSO4+H2SO4═Fe2(SO4)3+2H2O.
(3)已知:浓度均为0.1mol•L-1的金属阳离子,生成氢氧化物沉淀的pH如表:
步骤③的目的是将Fe2+氧化为Fe3+,并使Fe3+转化为Fe(OH)3沉淀而除去;
若在该浓度下除去铁的化合物,调节pH的最大范围是2.8≤pH<3.4.
(4)操作④发生反应的离子方程式为3Mn2++2MnO4-+2H2O═5MnO2↓+4H+;为了验证该操作所得固体中确实含有MnO2,可选用的试剂是浓盐酸和双氧水.
(5)操作⑤“一系列操作”,下列仪器中不需用的是B(填序号).
A.蒸发皿 B.坩埚 C.玻璃棒 D.酒精灯 E.漏斗.

请回答下列问题:
(1)加入过量稀硫酸溶解Al2O3的离子方程式是6H++Al2O3═2Al3++3H2O.
(2)流程中加入的KMnO4也可用H2O2代替,若用H2O2发生反应的化学方程式为H2O2+2FeSO4+H2SO4═Fe2(SO4)3+2H2O.
(3)已知:浓度均为0.1mol•L-1的金属阳离子,生成氢氧化物沉淀的pH如表:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
若在该浓度下除去铁的化合物,调节pH的最大范围是2.8≤pH<3.4.
(4)操作④发生反应的离子方程式为3Mn2++2MnO4-+2H2O═5MnO2↓+4H+;为了验证该操作所得固体中确实含有MnO2,可选用的试剂是浓盐酸和双氧水.
(5)操作⑤“一系列操作”,下列仪器中不需用的是B(填序号).
A.蒸发皿 B.坩埚 C.玻璃棒 D.酒精灯 E.漏斗.
17.下列说法正确的是( )
| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| B. | 分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种 | |
| C. | 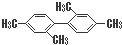 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | |
| D. | 1mol有机物 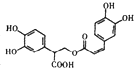 一定条件下能和7molNaOH反应 一定条件下能和7molNaOH反应 |
4.下列过程中,只破坏离子键的是( )
| A. | NO2被木炭吸附 | B. | NaHSO4加热至熔化 | ||
| C. | KHSO4晶体溶于水 | D. | Na2O2溶于水 |
1.用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压数值):
(1)用KSCN检验出Fe3+的现象是溶液变红.
(2)I中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应:2Cl--2e-=Cl2↑;.
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(4)II中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
①IV中检测Cl2的实验方法湿润的淀粉碘化钾试纸变蓝.
②与II对比,得出的结论(写出两点):加大电压cV以上时可以生成Cl2;阳极放电顺序Fe2+>Cl-.
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x>a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x>b | 电极附近出现黄色,无气泡产生 | 有Fe3+,无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+,无Cl2 |
(2)I中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应:2Cl--2e-=Cl2↑;.
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(4)II中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x>c | 无明显变化 | 有Cl2 |
| Ⅴ | c<x<b | 无明显变化 | 无Cl2 |
②与II对比,得出的结论(写出两点):加大电压cV以上时可以生成Cl2;阳极放电顺序Fe2+>Cl-.
18.下列说法中正确的是( )
| A. | 红热的铁丝在氯气中燃烧产生棕色的雾 | |
| B. | 含有氯元素的物质都呈黄绿色,均有毒 | |
| C. | 氢气在氯气中燃烧时,火焰显淡蓝色 | |
| D. | 氯水中滴入硝酸银溶液和稀硝酸后,产生白色沉淀 |
19.在强碱性溶液中,下列离子组能大量共存的是( )
| A. | Na+、K+、SO42-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |