题目内容
10.将表面有氧化膜的铝片伸入足量的NaOH溶液中,有关离子方程式正确的是( )| A. | Al2O3+OH-→AlO2-+H2O | B. | 2Al3++6OH-→2Al(OH)3↓ | ||
| C. | 2Al+2OH-+2H2O→2AlO2-+3H2↑ | D. | 2Al+6H2O→2Al3++6OH-+3H2↑ |
分析 将表面有氧化膜的铝片伸入足量的NaOH溶液中,氧化铝先与氢氧化钠反应生成偏铝酸钠和水,然后铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,据此书写离子方程式.
解答 解:将表面有氧化膜的铝片伸入足量的NaOH溶液中,氧化铝先与氢氧化钠反应生成偏铝酸钠和水,离子方程式:Al2O3+2OH-=2AlO2-+H2O;
然后铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故选:C.
点评 本题考查了离子方程式的书写,侧重考查与铝有关离子反应,明确铝、氧化铝的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
20.在25℃时,下列各种情况下一定能大量共存的离子组为( )
| A. | pH=7的溶液中:Fe3+、Cl-、Na+、NO3- | |
| B. | 由水电离出的c(H+)=1×10-13 mol•L-1的水溶液中Na+、CO32-、Cl-、K+ | |
| C. | 无色透明的酸性溶液中NH4+、NO3-、Al3+、Cl- | |
| D. | Al3+、HCO3-、I-、Ca2+ |
1.甲、乙、丙、X是中学化学中常见的4种物质,其转化关系如图,其中甲和X不可能是( )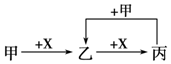

| A. | 甲为C2H5OH、X为O2 | B. | 甲为H2S、X为O2 | ||
| C. | 甲为HNO3、X为Fe | D. | 甲为AlCl3溶液、X为NaOH溶液 |
18.下列反应既是氧化还原反应,又是吸热反应的是( )
| A. | 铝粉与WO3共热制备金属钨 | B. | 高温下CO还原Fe2O3制备铁 | ||
| C. | 铁粉与水蒸气加热制备氢气 | D. | Ca( OH)2与NH4Cl加热制备氨气 |
5.重水(${\;}_{1}^{2}$H2O)是重要的核工业原料,关于氘原子(${\;}_{1}^{2}$H)说法错误的是( )
| A. | 氘原子核外有1个电子 | B. | 氘原子质量数为2 | ||
| C. | 一个氘原子中含有2个中子 | D. | 与氕原子互为同位素 |
15.只用组内溶液相互混合就能鉴别的组别是( )
| A. | Na2SO4、BaCl2、KNO3、NaCl | B. | NaCl、AgNO3、NaNO3、HCl | ||
| C. | NaOH、Na2SO4、FeCl3、MgCl2 | D. | Na2SO4、NaNO3、CaCl2、NaCl |
6.向体积相同的MgSO4、CuSO4、Fe2(SO4)3溶液加入物质的量浓度相同的NaOH溶液,恰好完全反应,若消耗NaOH溶液的体积比为3:2:1,则上述三种溶液的物质的量浓度之比为( )
| A. | 9:6:1 | B. | 3:2:1 | C. | 6:3:2 | D. | 1:2:3 |
3.下列说法中,正确的是( )
| A. | 乙烷、乙烯、乙炔都难溶于水,且密度比水小 | |
| B. | 可用溴水来鉴别乙烷、乙烯和乙炔三种无色气体 | |
| C. | 在一定条件下,乙烷、乙烯、乙炔都能与氯气发生同类型反应 | |
| D. | 乙烷、乙烯、乙炔都能发生加聚反应生成高分子化合物 |
4.下列有关物质的保存方法不正确的是( )
| A. | 浓氨水、浓硝酸应保存在棕色试剂瓶中,并置于阴凉处 | |
| B. | 液溴易挥发,应保存在棕色试剂瓶中,并加水封 | |
| C. | 在储存铵态化肥时,应密封包装并放在阴凉通风处 | |
| D. | 碘易升华,应保存在棕色细口瓶中,并置于阴凉处 |