题目内容
6.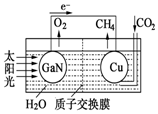 科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.
科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.①写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O.
②为提高该人工光合系统的工作效率,可向装置中加入少量硫酸(选填“氢氧化钠”或“硫酸”).
分析 ①原电池中电子从负极流向正极,则Cu电极为正极,正极上CO2得电子生成CH4;
②根据溶液中的电解质的酸碱性判断.
解答 解:①原电池中电子从负极流向正极,则Cu电极为正极,正极上CO2得电子生成CH4,则铜电极表面的电极反应式为:CO2+8e-+8H+=CH4+2H2O;
故答案为:CO2+8e-+8H+=CH4+2H2O;
②电解质溶液显酸性,加氢氧化钠能与二氧化碳反应,所以不能加NaOH,应该加硫酸;
故答案为:硫酸.
点评 本题考查化学电源新型电池,题目难度中等,明确原电池原理为解答根据,注意正确判断电极反应、电子流向、离子流向,难点是电极反应式的书写.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
17.下列关于镁和钠的比较,结论正确的是( )
| A. | 铝镁合金的硬度较大,钠钾合金常温下为液态 | |
| B. | 因为钠的金属性比镁要强,所以钠的熔点比镁要高 | |
| C. | 镁能置换硫酸铜溶液中的铜,钠也能置换硫酸铜溶液中的铜 | |
| D. | 在空气中都能被点燃,生成的产物都是氧化物,氧在产物中的化合价都是-2 |
14. 某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
 某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )| A. | 该电池为原电池装置 | |
| B. | a与外接电源正极相连 | |
| C. | a电极的电极反应式为2CO2+6H++12e-═C2H5OH+3H2O | |
| D. | 当a电极上生成1 mol C2H5OH时,b电极上产生标准状况下的气体体积为67.2 L |
1.下列试验中,所选装置不合理的是( )
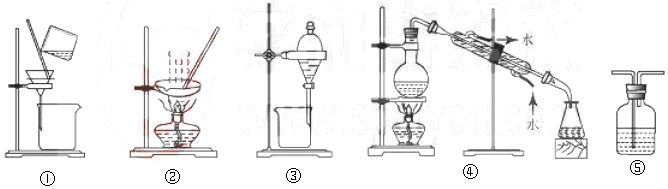

| A. | 粗盐提纯,选①和② | B. | 用CC14提取碘水中的碘,选③ | ||
| C. | 用NaOH溶液吸收少量C12选⑤ | D. | 分离Na2CO3溶液和CH3COOC2H5,选④ |
11.在钠和水的反应实验中,你观察不到的现象是( )
| A. | 酚酞试液从无色变为红色 | B. | 钠安静地浮在水面上 | ||
| C. | 钠熔化成光亮的小球 | D. | 钠在水面上到处游动 |
18.下列反应的离子方程式可用H++OH-=H2O表示的有( )
| A. | 醋酸与氢氧化钾溶液 | B. | 氢氧化铜和盐酸 | ||
| C. | 硫酸氢钠与氨水溶液 | D. | 硝酸与氢氧化钡溶液 |
15.下列叙述正确的是( )
| A. | 常温下,0.1 mol•L-1 pH=8的NaHB溶液中:c(HB-)>c(B2-)>c(H2B) | |
| B. | pH=12氨水溶液与pH=2盐酸溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 相同物质的量浓度的下列溶液中:①NH4Al(SO4)2②NH4Cl③CH3COONH4④c(NH3•H2O);c(NH4+)由大到小的顺序是:①>②>③>④ | |
| D. | 某二元酸(H2A)在水中的电离方程式为:H2A=H++HA-,HA-?H++A2-则在NaHA溶液中:c(Na+)=c(HA-)+c(A2-)+c(H2A) |
16.下列不能使红墨水褪色的是( )
| A. | 氯水 | B. | 次氯酸钠溶液 | C. | 活性炭 | D. | 氯化钙溶液 |