题目内容
用已知浓度的盐酸测定未知浓度的NaOH溶液的物质的量浓度,进行酸碱中和滴定时,无论是酸往碱中滴还是碱往酸中滴,下列操作都会使测定结果偏低的是(锥形瓶中溶液用滴定管量取)( )
| A、酸式滴定管未用标准盐酸润洗 |
| B、滴定过程中不慎有液体溅出 |
| C、滴定前仰视读数,滴定后读数正确 |
| D、碱式滴定管未用待测液润洗 |
考点:中和滴定
专题:电离平衡与溶液的pH专题
分析:根据c(碱)=
分析,以此判断浓度的误差.
| c(酸)×V(酸) |
| V(碱) |
解答:
解:A.酸式滴定管未用待测盐酸润洗,则酸液被稀释,若碱往酸中滴,造成消耗的V(碱)偏小,根据c(碱)=
分析可知c(碱)偏小;若酸往碱中滴,造成消耗的V(酸)偏大,根据c(碱)=
分析,可知c(碱)偏大,故A错误;
B.滴定过程中锥形瓶中不慎有液体溅出,若碱往酸中滴,造成消耗的V(碱)偏大,根据c(碱)=
分析,可知c(碱)偏小;若酸往碱中滴,造成消耗的V(酸)偏大,根据c(碱)=
分析,可知c(碱)偏大,故B错误;
C.滴定前仰视读数,滴定后读数正确,若碱往酸中滴,导致的V(碱)偏小,根据c(碱)=
分析,可知c(碱)偏大;若酸往碱中滴,造成消耗的V(酸)偏小,根据c(碱)=
分析,可知c(碱)偏小,故C错误;
D.碱式滴定管未用待测液润洗,碱被稀释,浓度偏小,若碱往酸中滴,造成消耗的V(碱)偏大,根据c(碱)=
分析,可知c(碱)偏小;若酸往碱中滴,造成消耗的V(酸)偏小,根据c(碱)=
分析,可知c(碱)偏小,故D正确,
故选D.
| c(酸)×V(酸) |
| V(碱) |
| c(酸)×V(酸) |
| V(碱) |
B.滴定过程中锥形瓶中不慎有液体溅出,若碱往酸中滴,造成消耗的V(碱)偏大,根据c(碱)=
| c(酸)×V(酸) |
| V(碱) |
| c(酸)×V(酸) |
| V(碱) |
C.滴定前仰视读数,滴定后读数正确,若碱往酸中滴,导致的V(碱)偏小,根据c(碱)=
| c(酸)×V(酸) |
| V(碱) |
| c(酸)×V(酸) |
| V(碱) |
D.碱式滴定管未用待测液润洗,碱被稀释,浓度偏小,若碱往酸中滴,造成消耗的V(碱)偏大,根据c(碱)=
| c(酸)×V(酸) |
| V(碱) |
| c(酸)×V(酸) |
| V(碱) |
故选D.
点评:本题主要考查了中和滴定操作的误差分析,根据c(碱)=
分析是解答的关键,题目难度不大.
| c(酸)×V(酸) |
| V(碱) |

练习册系列答案
相关题目
下列说法正确的是( )
A、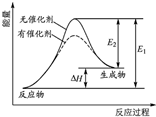 某反应的反应过程中能量变化如图所示,由如图分析可知催化剂不改变反应的焓变 | ||||||||||
| B、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | ||||||||||
C、已知:
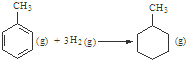 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 | ||||||||||
| D、常温下在0.10 mol?L-1的氨水中加入少量NH4Cl晶体,NH3?H2O的电离程度和溶液的pH均减小 |
关于物质分类的正确组合是( )
| 组合分类 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | 纯碱 | 盐酸 | 烧碱 | 氧化铝 | 二氧化碳 |
| B | 烧碱 | 硫酸 | 食盐 | 氧化镁 | 一氧化碳 |
| C | 苛性钠 | 醋酸 | 碳酸铵 | 过氧化钠 | 二氧化硫 |
| D | 苛性钾 | 盐酸 | 小苏打 | 氧化钠 | 三氧化硫 |
| A、A | B、B | C、C | D、D |
若用已知浓度的碳酸钠溶液来测定某盐酸溶液的浓度,配制碳酸钠溶液所用碳酸钠中分别含有如下杂质:
①NaOH②NaHCO3③NaCl④K2CO3.所测结果偏低的是( )(已知相对原子质量:H 1,C 12,O 16,Na 23,Cl 35.5 K 39)
①NaOH②NaHCO3③NaCl④K2CO3.所测结果偏低的是( )(已知相对原子质量:H 1,C 12,O 16,Na 23,Cl 35.5 K 39)
| A、① | B、② | C、②③ | D、③④ |
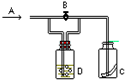 如图所示,A处通入潮湿的Cl2,关闭B阀时,C处干燥的红色布条无变化; 打开B阀时,C处干燥的红色布条褪色,则D中的溶液是( )
如图所示,A处通入潮湿的Cl2,关闭B阀时,C处干燥的红色布条无变化; 打开B阀时,C处干燥的红色布条褪色,则D中的溶液是( )| A、浓盐酸 |
| B、H2O |
| C、NaOH溶液 |
| D、饱和食盐水 |