题目内容
19.关于化学对社会进步和人类文明的贡献,下列说法不正确的是( )| A. | 化石燃料的直接利用,促进了低碳经济的发展 | |
| B. | 新材料的研制和应用,提高了人们的生活品质 | |
| C. | 合成药物的研发和使用,促进了医疗卫生事业的发展 | |
| D. | 化肥的合理使用提高了农作物产量,缓解了人类粮食危机 |
分析 A、化石燃料的燃烧造成大量的二氧化碳的排放以及二氧化硫等排放,不完全燃烧时会产生一氧化碳等;
B、合成新材料利于改善环境和生活质量;
C、合成药物,能够治疗疾病,改善某些元素的不足,改善生活质量,属于化学研究的范围;
D、农药和化肥是农业稳定粮食生产的保证,对于提高质量和产量,改善品质都有好处.
解答 解:A、化石燃料的直接利用,抑制了低碳经济的发展,该选项说法不正确,故A错误;
B、新材料的研制和应用,提高了人们的生活品质,故B正确;
C、合成药物的研发和使用,保障了人体健康,故C正确;
D、化肥的合理使用提高了农作物产量,缓解了人类粮食危机,故D正确;
故选A.
点评 本题考查了常见生活环境污染及其治理的分析,化学是研究物质的组成、结构、性质及其变化规律的科学,我们研究物质的目的是为了应用,了解化学的用途有利于培养学习兴趣,提高社会责任感.注意知识积累,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目
9.二氧化硫是一种重要的化工原料,主要用于生产硫酸、亚硫酸盐等.请回答:
(1)已知2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的关键反应.如图1为不同温度(T1、T2)下SO2的转化率随时间的变化曲线.
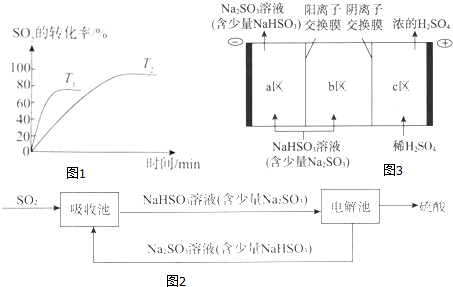
①T1>(填“>”“<”或“=”)T2,判断的依据是温度越高反应速率越快,达到化学平衡的时间越短;该反应为放(填“放”或“吸”)热反应,判断的依据是温度升高时平衡向吸热方向移动,SO2的转化率减小.
②如表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率.
i.b对应的投料比为4:15.
ii.投料比为8:10时,平衡混合气体中SO3体积分数为50%.
(2)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如图2:
①吸收池中发生反应的离子方程式是SO2+SO32-+H2O=2HSO3-.
②电解池的构造示意图如图3:
i.在图中标示出b区的Na+和HSO3-的移动方向.
ii.请结合生成H2SO4的电极反应式说明c区除得到浓的硫酸外,还会得到什么物质:SO2.
(1)已知2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的关键反应.如图1为不同温度(T1、T2)下SO2的转化率随时间的变化曲线.

①T1>(填“>”“<”或“=”)T2,判断的依据是温度越高反应速率越快,达到化学平衡的时间越短;该反应为放(填“放”或“吸”)热反应,判断的依据是温度升高时平衡向吸热方向移动,SO2的转化率减小.
②如表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率.
| 投料比 | a | b | c | d |
| SO2平衡转化率/% | 97.1 | 96.8 | 95.8 | 90.0 |
ii.投料比为8:10时,平衡混合气体中SO3体积分数为50%.
(2)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如图2:
①吸收池中发生反应的离子方程式是SO2+SO32-+H2O=2HSO3-.
②电解池的构造示意图如图3:
i.在图中标示出b区的Na+和HSO3-的移动方向.
ii.请结合生成H2SO4的电极反应式说明c区除得到浓的硫酸外,还会得到什么物质:SO2.
10.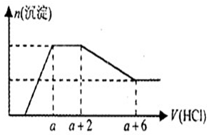 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )| A. | 原溶液中一定含有Na2SO4 | |
| B. | 反应后形成的溶液溶质为NaCl | |
| C. | 原溶液中含有CO32-与AlO2-的物质的量比为1:1 | |
| D. | 原溶液中一定含有的离子是OH-,CO32-,SiO32-,AlO2- |
7.有NO、CO2、N2O4三种气体,它们分别都含有0.5mol氧原子,则三种气体的物质的量之比为( )
| A. | 1:2:4 | B. | 1:1:1 | C. | 4:2:1 | D. | 1:2:4 |
11.科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空.如图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导正极生成的O2-.下列叙述错误的是( )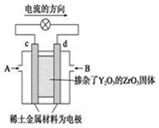

| A. | c电极是正极,发生还原反应 | |
| B. | B口通入的是甲烷,发生氧化反应 | |
| C. | 放电时O2-离子向d极移动 | |
| D. | d极上的电极反应式为:CH4+4O2-+8e-=CO2↑+2H2O |
9.根据下列标准,分类合理的是( )
| A. | 根据物质的组成元素是否单一,将纯净物分为单质和化合物 | |
| B. | 根据反应中的能量变化,将化学反应分为氧化还原反应、非氧化还原反应 | |
| C. | 根据电解质溶液导电能力强弱,将电解质分为强电解质、弱电解质 | |
| D. | 根据变化过程中是否有化学键的断裂,将物质变化分为物理变化和化学变化 |