题目内容
17.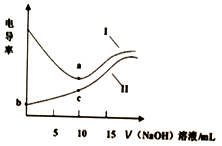 用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )
用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )| A. | b点pH值大于1 | B. | 盐酸浓度为 0.lmol•L-1 | ||
| C. | c点:c(Na+)>c(A-)>c(H+)>c(OH-) | D. | 曲线Ⅰ为盐酸,曲线Ⅱ为醋酸溶液 |
分析 溶液导电能力与离子浓度成正比,CH3COOH是弱电解质,溶液中离子浓度较小,加入NaOH后,溶液中离子浓度增大,溶液导电性增强;HCl是强电解质,随着NaOH溶液加入,溶液体积增大,导致溶液中离子浓度减小,溶液导电能力减弱,当完全反应式离子浓度最小,继续加入NaOH溶液,离子浓度增大,溶液导电能力增强,根据图知,曲线Ⅰ代表0.1 mol/L NaOH溶液滴定HC1溶液的滴定曲线,曲线Ⅱ代表0.1 mol/LNaOH溶液滴定CH3COOH溶液的滴定曲线,据此分析.
解答 解:A.曲线Ⅱ为醋酸溶液,所以b点pH值大于1,故A正确;
B.曲线Ⅱ当盐酸与氢氧化钠恰好完全反应时离子浓度最小,而此时消耗氢氧化钠的体积为10mL,所以盐酸浓度为 0.lmol•L-1,故B正确;
C.c点是醋酸与氢氧化钠恰好完全反应生成醋酸钠,溶液呈碱性,所以离子浓度的大小为:c(Na+)>c(A-)>c(OH-)>c(H+),故C错误;
D.由分析可知曲线Ⅰ代表盐酸,曲线Ⅱ代表醋酸溶液,故D正确;
故选C.
点评 本题以电导率为载体考查离子浓度大小比较、盐类水解等知识点,题目难度中等,明确混合溶液中溶质及其性质、溶液导电性强弱影响因素是解本题关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
6.将 6.4g 铜与 140mL 一定浓度的硝酸反应,铜完全溶解产生的 NO 和 NO2混合气体的体积为 3.36L(标准状况),其中 NO 的体积为(标准状况)( )
| A. | 0.56 L | B. | 1.344 L | C. | 2.016 L | D. | 2.8 L |
8.常温下,向1LpH=10的KOH溶液中持续通入CO2,与溶液中水电离出的c(OH-)与通入的CO2的体积(V)关系如图所示.下列叙述不正确的是( )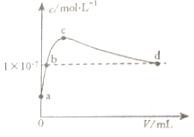

| A. | b点溶液呈中性 | |
| B. | d点溶液中:c(K+)=2c(CO32-)+c(HCO3-) | |
| C. | c点溶液中:2c(H2CO3)+c(H+)+c(HCO3-)=c(OH-) | |
| D. | a点溶液中:水电离出的c(H+)=1×10-10mol•L-1 |
5.化学与社会、生活密切相关.对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 光线透过树叶间的缝隙射入密林中时,会产生一道道光柱 | 气溶胶产生的丁达尔效应 |
| B | 炒菜时加碘盐要在菜准备出锅时添加 | 食盐中的碘受热易升华 |
| C | 明矾常用作净水剂 | 明矾具有杀菌消毒功能 |
| D | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | 水果中的葡萄糖能与高锰酸钾发生氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
12.化学在生活中有着广泛的应用,下列物质的性质与用途对应关系错误的是( )
| 物质 | 性质 | 用途 | |
| A | Fe2O3 | 红棕色粉末 | 常用作红色油漆和颜料 |
| B | NaHCO3 | 溶液呈碱性 | 可用作食用碱或工业用碱 |
| C | Si | 导电性介于道题与绝缘体之间 | 用于制作计算机芯片、光电池 |
| D | SO2 | 还原性 | 工业上用来漂白纸浆、毛、丝、草帽辫等 |
| A. | A | B. | B | C. | C | D. | D |
2.已知 25℃下时,NH3•H2O kb=1.77×10-5;H2CO3 ka1=4.30×10-7、ka2=5.61×10-11. 25℃时有关NH4HCO3溶液的说法中正确的是( )
| A. | 呈弱酸性 | |
| B. | c(OH-)+c(NH3•H2O)=c(H+)+c(H2CO3) | |
| C. | 滴入NaOH 溶液发生反应:NH4++OH-=NH3•H2O和HCO3-+OH-=H2O+CO32- | |
| D. | 滴入NaOH溶液,则$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$增大 |
9.向3mol•L-1盐酸中加入打磨后的镁条,一段时间后生成灰白色固体X,并测得反应后溶液pH升高.为确认固体X的成分,过滤洗涤后进行实验:
①向固体X中加入足量硝酸,固体溶解,得到无色溶液,将其分成两等份;
②向其中一份无色溶液中加入足量AgNO3溶液,得到白色沉淀a;
③向另一份无色溶液中加入足量NaOH溶液,得到白色沉淀b.
下列分析不正确的是( )
①向固体X中加入足量硝酸,固体溶解,得到无色溶液,将其分成两等份;
②向其中一份无色溶液中加入足量AgNO3溶液,得到白色沉淀a;
③向另一份无色溶液中加入足量NaOH溶液,得到白色沉淀b.
下列分析不正确的是( )
| A. | 溶液pH升高的主要原因:Mg+2H+═Mg2++H2↑ | |
| B. | 生成沉淀a的离子方程式:Ag++Cl-═AgCl↓ | |
| C. | 沉淀b是Mg(OH)2 | |
| D. | 若a、b的物质的量关系为n(a):n(b)=1:3,则可推知固体X的化学式为Mg3(OH)6Cl |
6.化学与社会、生活密切相关.对下列现象或事实及解释均正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 化石燃料燃烧时采取脱硫措施 | 提高化石燃料的利用率 |
| B | 食品袋中常放有硅胶和铁粉,都能起到干燥的作用 | 二者都有较强的吸水性 |
| C | 高温加热能杀死流感病毒 | 蛋白质受热变性 |
| D | 高铁车厢采用铝合金材料 | 铝和氧气不反应 |
| A. | A | B. | B | C. | C | D. | D |
 创新发展材料技术可推动人类社会进步.
创新发展材料技术可推动人类社会进步.