题目内容
 氧化还原反应规律是化学学科的重要规律之一.按要求回答下列问题:
氧化还原反应规律是化学学科的重要规律之一.按要求回答下列问题:(1)被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑,此反应中B元素的化合价没有发生变化,则NaBH4中H的化合价为
(2)有下列三个反应:①Cl2+FeI2=FeCl2+I2;②2Fe2++Br2=2Fe3++2Br-;
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
①根据以上方程式可以得到Fe2+、Co2+、Br-、I-还原性由强的弱的顺序为
②1molCo2O3能氧化HCl的物质的量
(3)完成并配平下列化学反应方程式:□KMnO4+□H2C2O4+□
(4)一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2H++Zn=Zn2++H2↑,可拆写为氧化反应式:Zn-2e-=Zn2+,还原反应式:2H++2e-=H2↑.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
①将2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”:其中,氧化反应式为
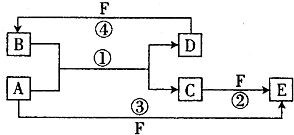
②由①中的反应,可设计成如图所示的原电池:若电极a为Cu,电解质溶液甲的化学式为
考点:氧化还原反应,氧化还原反应方程式的配平,原电池和电解池的工作原理
专题:氧化还原反应专题,电化学专题
分析:(1)NaBH4+2H2O=NaBO2+4H2↑中,B元素的化合价没有发生变化,B为+3价,则NaBH4中H的化合价为-1价,该反应中H元素的化合价由-1价升高为0,H元素的化合价由+1价降低为0;
(2)①含元素化合价升高的物质为还原剂,还原剂的还原性大于还原产物的还原性;
②Co2O3+6HCl=2CoCl2+Cl2↑+3H2O中,6molHCl中只有2mol作还原剂;
(3)KMnO4+H2C2O4+□→CO2+K2SO4+MnSO4+H2O,由原子守恒可知,反应物中有硫酸,Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,结合电子守恒及原子守恒配平;
(4)①将2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”,氧化反应中Cu失去电子;
②由①中的反应,可设计成如图所示的原电池:若电极a为Cu,a为阳极,b为阴极,阴极上铁离子得到电子,图中溶液甲中含铜离子.
(2)①含元素化合价升高的物质为还原剂,还原剂的还原性大于还原产物的还原性;
②Co2O3+6HCl=2CoCl2+Cl2↑+3H2O中,6molHCl中只有2mol作还原剂;
(3)KMnO4+H2C2O4+□→CO2+K2SO4+MnSO4+H2O,由原子守恒可知,反应物中有硫酸,Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,结合电子守恒及原子守恒配平;
(4)①将2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”,氧化反应中Cu失去电子;
②由①中的反应,可设计成如图所示的原电池:若电极a为Cu,a为阳极,b为阴极,阴极上铁离子得到电子,图中溶液甲中含铜离子.
解答:
解:(1)NaBH4+2H2O=NaBO2+4H2↑中,B元素的化合价没有发生变化,B为+3价,则NaBH4中H的化合价为-1价,该反应中H元素的化合价由-1价升高为0,H元素的化合价由+1价降低为0,则氧化产物、还原产物均为H2,
故答案为:-1,H2;H2;
(2)①还原剂的还原性大于还原产物的还原性可知,还原性为I->Fe2+>Br->Co2+,故答案为:I->Fe2+>Br->Co2+;
②Co2O3+6HCl=2CoCl2+Cl2↑+3H2O中,6molHCl中只有2mol作还原剂,则1molCo2O3能氧化HCl的物质的量为2mol,故答案为:2mol;
(3)KMnO4+H2C2O4+□→CO2+K2SO4+MnSO4+H2O,由原子守恒可知,反应物中有硫酸,Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,由电子守恒及原子守恒可知,该反应为2KMnO4+5H2C2O4+3 H2SO4=10CO2+K2SO4+2MnSO4+8H2O,
故答案为:H2SO4;2KMnO4+5H2C2O4+3 H2SO4=10CO2+K2SO4+2MnSO4+8H2O;
(4)①将2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”,氧化反应中Cu失去电子,氧化反应为Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
②由①中的反应,可设计成如图所示的原电池:若电极a为Cu,a为阳极,图中溶液甲中含铜离子,可选择CuSO4,b为阴极,阴极上铁离子得到电子,b上的电极反应式为2Fe3++2e-=2Fe2+,故答案为:CuSO4;2Fe3++2e-=2Fe2+.
故答案为:-1,H2;H2;
(2)①还原剂的还原性大于还原产物的还原性可知,还原性为I->Fe2+>Br->Co2+,故答案为:I->Fe2+>Br->Co2+;
②Co2O3+6HCl=2CoCl2+Cl2↑+3H2O中,6molHCl中只有2mol作还原剂,则1molCo2O3能氧化HCl的物质的量为2mol,故答案为:2mol;
(3)KMnO4+H2C2O4+□→CO2+K2SO4+MnSO4+H2O,由原子守恒可知,反应物中有硫酸,Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,由电子守恒及原子守恒可知,该反应为2KMnO4+5H2C2O4+3 H2SO4=10CO2+K2SO4+2MnSO4+8H2O,
故答案为:H2SO4;2KMnO4+5H2C2O4+3 H2SO4=10CO2+K2SO4+2MnSO4+8H2O;
(4)①将2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”,氧化反应中Cu失去电子,氧化反应为Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
②由①中的反应,可设计成如图所示的原电池:若电极a为Cu,a为阳极,图中溶液甲中含铜离子,可选择CuSO4,b为阴极,阴极上铁离子得到电子,b上的电极反应式为2Fe3++2e-=2Fe2+,故答案为:CuSO4;2Fe3++2e-=2Fe2+.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念、还原性比较及原电池的考查,注意原电池与氧化还原反应的关系,题目难度不大.

练习册系列答案
相关题目
下列装置或操作不能达到实验目的是( )
A、 实验室制取氯气 |
B、 Fe(OH)2的制取 |
C、 氨气的制取 |
D、 检查装置气密性 |
下列说法可充分说明反应P(g)+Q(g)?S(g)+R(g),在恒温、恒容密闭容器中的反应已达平衡状态的是( )
| A、容器里P、Q、R、S四种物质共存 |
| B、单位时间内消耗n mol P同时生成n mol S |
| C、容器内气体压强、密度不随时间变化 |
| D、容器里Q、R的体积分数不再改变 |
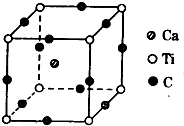 短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p亚层与所有s亚层电子总数相等,D元素原子的L层的p亚层中有3个未成对电子.
短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p亚层与所有s亚层电子总数相等,D元素原子的L层的p亚层中有3个未成对电子. W、X、Y、Z、R为前四周期元素且原子序数依次增大.W与Y形成常温下呈液态的化合物G,X可以spm(m=1,2,3)杂化方式与X形成一系列X的化合物,X的单质在高温条件下与G反应生成W单质和气态化合物;W的单质与Z的单质在点燃或光照时均能反应生成1:1的水溶液为常见的酸;R原子的价电子层的未成对电子数为4.回答下列问题:
W、X、Y、Z、R为前四周期元素且原子序数依次增大.W与Y形成常温下呈液态的化合物G,X可以spm(m=1,2,3)杂化方式与X形成一系列X的化合物,X的单质在高温条件下与G反应生成W单质和气态化合物;W的单质与Z的单质在点燃或光照时均能反应生成1:1的水溶液为常见的酸;R原子的价电子层的未成对电子数为4.回答下列问题: 铁、铝、铜及其化合物在生产、生活中有广泛的用途,试回答下列问题:
铁、铝、铜及其化合物在生产、生活中有广泛的用途,试回答下列问题: