题目内容
25mL1.0mol/LH2SO4溶液与足量锌反应,在标准状况下产生H2多少升?生成硫酸锌的物质的量为多少?
考点:化学方程式的有关计算
专题:计算题
分析:锌与硫酸反应生成硫酸锌与氢气,根据n=c×v和Zn+H2SO4═ZnSO4+H2↑可计算H2、硫酸锌的物质的量,再利用V=nVm计算氢气的体积.
解答:
解:25mL1.0mol/LH2SO4溶液n(H2SO4)=c×v=1.0mol/L×0.025L=0.025mol,与足量锌反应,
Zn+H2SO4 ═ZnSO4 +H2↑
1mol 1mol 1mol
0.025mol 0.025mol 0.025mol
故生成氢气的体积为V=n×Vm=0.025mol×22.4L/mol═0.56L,生成硫酸锌的物质的量为0.025mol,
答:在标准状况下产生H20.56L;生成硫酸锌0.025 mol.
Zn+H2SO4 ═ZnSO4 +H2↑
1mol 1mol 1mol
0.025mol 0.025mol 0.025mol
故生成氢气的体积为V=n×Vm=0.025mol×22.4L/mol═0.56L,生成硫酸锌的物质的量为0.025mol,
答:在标准状况下产生H20.56L;生成硫酸锌0.025 mol.
点评:本题考查根据方程式进行的计算,题目难度不大,侧重对基础知识的巩固,注意基础知识的理解掌握.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
6027Co是一种放射性原子,6027Co原子核内中子数为( )
| A、60 | B、33 | C、87 | D、27 |
下列各项中表达正确的是( )
| A、一个D2O分子所含的中子数为10 | ||
B、NH4I的电子式: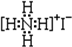 | ||
C、CO2的分子模型: | ||
D、中子数为20的核素:
|
NA表示阿伏加德常数,下列说法正确的是( )
| A、2.24L HCl气体中含有0.1NA个HCl分子 |
| B、室温下,1molCH4含有的电子数为10NA |
| C、将0.1mol FeCl3溶于1L水中,所得溶液中含有0.1NA个Fe3+ |
| D、25℃时,1LpH=13的Ba(OH)2溶液中含有0.2NA个OH- |
下列叙述正确的是( )
| A、纯碱、烧碱均属碱 |
| B、CO、SO2均属酸性氧化物 |
| C、凡能电离出H+的化合物均属酸 |
| D、盐类物质一定含有金属离子或铵根离子 |