题目内容
关于乙醇结构与性质的说法中正确的是( )
| A、乙醇结构中有-OH,其水溶液可以电离出OH-而显碱性 |
| B、乙醇与乙酸在一定条件下反应生成乙酸乙酯 |
| C、乙醇与钠反应可以产生氢气,所以乙醇显酸性 |
| D、乙醇与钠反应比较平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼 |
考点:有机物的结构和性质
专题:
分析:A、乙醇的官能团是羟基,能与水形成氢键,易溶于水,但不能电离出OH-;
B、乙醇与乙酸在浓硫酸存在条件下加热反应生成乙酸乙酯和水;
C、乙醇的溶液为中性溶液,不能电离出氢离子;
D、羟基氢原子的活泼性不同,反应进行的剧烈程度不同,水是弱电解质,乙醇是非电解质.
B、乙醇与乙酸在浓硫酸存在条件下加热反应生成乙酸乙酯和水;
C、乙醇的溶液为中性溶液,不能电离出氢离子;
D、羟基氢原子的活泼性不同,反应进行的剧烈程度不同,水是弱电解质,乙醇是非电解质.
解答:
解:A、乙醇结构中有-OH,能与水形成氢键,所以乙醇溶解于水,但不能电离出OH-,故A错误;
B、乙醇和乙酸在浓硫酸做催化剂、吸水剂的条件下加热反应生成乙酸乙酯和水,故B正确;
C、乙醇与钠反应可以产生氢气,但乙醇为非电解质,不能电离出氢离子,其溶液不显酸性,故C错误;
D、水是弱电解质,乙醇是非电解质,乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼,故D正确;
故选BD.
B、乙醇和乙酸在浓硫酸做催化剂、吸水剂的条件下加热反应生成乙酸乙酯和水,故B正确;
C、乙醇与钠反应可以产生氢气,但乙醇为非电解质,不能电离出氢离子,其溶液不显酸性,故C错误;
D、水是弱电解质,乙醇是非电解质,乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼,故D正确;
故选BD.
点评:本题考查了有机物结构与性质,侧重考查乙酸、乙醇的结构与性质,题目难度不大,注意掌握常见有机物结构与性质,明确乙醇为非电解质,钠与乙醇的反应不如钠与水的反应剧烈.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列将饱和碘水中的碘单质分离出来的实验操作说法正确的是( )
| A、应该使用萃取的方法,并选用酒精作萃取剂 |
| B、萃取使用的主要仪器是分液漏斗,在使用前要先检验其是否漏液 |
| C、静置分层后碘单质一定溶在上层液体中,应从分液漏斗的上口倒出 |
| D、从分液漏斗中分离出的就是纯净的碘单质 |
一定条件下反应2AB(g)?A2(g)+B2(g)达到平衡状态的标志是( )
| A、单位时间内生成nmolA2,同时消耗2n molAB |
| B、容器内,3种气体AB、A2、B2共存 |
| C、容器的总压强不变 |
| D、容器中各组分的体积分数不随时间变化 |
下表为部分一氯代烷的结构简式和一些性质数据.下列对表中物质与数据的分析归纳错误的是( )
| 序号 | 结构简式 | 沸点/℃ | 相对密度 |
| ① | CH3Cl | -24.2 | 0.915 9 |
| ② | CH3CH2Cl | 12.3 | 0.897 8 |
| ③ | CH3CH2CH2Cl | 46.6 | 0.890 9 |
| ④ | CH3CHClCH3 | 35.7 | 0.861 7 |
| ⑤ | CH3CH2CH2CH2Cl | 78.44 | 0.886 2 |
| ⑥ | CH3CH2CHClCH3 | 68.2 | 0.873 2 |
| ⑦ | (CH3)3CCl | 52 | 0.842 0 |
| A、物质①②③⑤可互相称为同系物 |
| B、一氯代烷同分异构体的沸点随着支链的增多而升高 |
| C、一氯代烷的沸点随着碳数的增多而趋于升高 |
| D、一氯代烷的相对密度随着碳数的增多而趋于减小 |
在下列反应中,HCl 所起的作用( )
①NaOH+HCl=NaCl+H2O
②Zn+2HCl=ZnCl2+H2↑
③MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑
④CuO+2HCl=CuCl2+H2O.
①NaOH+HCl=NaCl+H2O
②Zn+2HCl=ZnCl2+H2↑
③MnO2+4HCl(浓)
| ||
④CuO+2HCl=CuCl2+H2O.
| A、①④表现出酸性 |
| B、①②表现出氧化性 |
| C、③既表现出氧化性又表现出酸性 |
| D、③④表现出还原性 |
下列叙述正确的是( )
A、常温下,将pH=11的氨水和pH=3的盐酸,等体积混合后,所得溶液中各离子浓度的关系是c(Cl-)>c(NH
| ||
| B、某二元酸在水中的电离方程式为:H2B═H++HB-,HB-?H++B2-,所以NaHB溶液呈酸性 | ||
| C、在BaSO4饱和溶液中加入少量的BaCl2溶液产生沉淀,平衡后的溶液中:C(Ba2+)?C(SO42-)>Ksp;c(Ba2+)>C(SO42-) | ||
| D、等浓度的NH3?H2O、NH4HSO4,NH4Cl溶液中c(NH4+)在逐渐增大 |
水溶液中能大量共存的一组离子是( )
| A、Na+、OH-、Cl-、HCO3- |
| B、H+、Na+、Fe2+、MnO4- |
| C、K+、Ca2+、Cl-、NO3- |
| D、K+、NH4+、OH-、SO42- |
已知14mol/L的硫酸溶液的溶质的质量分数为80%,那么7mol/L的硫酸溶液的溶质的质量分数将( )
| A、大于40% | B、等于40% |
| C、小于40% | D、无法确定 |
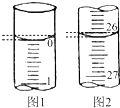 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白: