题目内容
13.M是一种化工原料,可以制备一系列物质(见如图).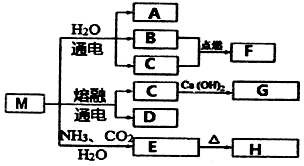
下列说法正确的是( )
| A. | 元素C、D形成的简单离子半径,前者大于后者 | |
| B. | F的热稳定性比H2S弱 | |
| C. | 化合物A、F中化学键的类型相同 | |
| D. | 元素C、D的最高价氧化物的水化物均可以和H发生反应 |
分析 M为化工原料,电解M生成C与氢氧化钙反应,可知M中含活泼金属,且M与水电解生成B、C可点燃下反应,M→E→F为纯碱工业发生的转化,则M为NaCl,A为NaOH,B为H2,C为Cl2,F为HCl,D为Na,G为漂白粉,E为NaHCO3,H为Na2CO3,以此来解答.
解答 解:由上述分析可知,M为NaCl,A为NaOH,B为H2,C为Cl2,F为HCl,D为Na,E为NaHCO3,H为Na2CO3,
A.C的阴离子有3个电子层,D的阳离子有2个电子层,则元素C、D形成的简单离子半径,前者大于后者,故A正确;
B.非金属性Cl>S,F的热稳定性比H2S强,故B错误;
C.A含离子键和O-H共价键,F只含共价键,故C错误;
D.C、D的最高价氧化物的水化物分别为高氯酸、NaOH,NaOH与H不反应,故D错误;
故选A.
点评 本题考查无机物的推断,为高频考点,把握图中转化、电解及纯碱工业来推断物质为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列表示对应化学反应的离子方程式,正确的是( )
| A. | FeCl3溶液和Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 醋酸溶液水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | NO2与氢氧化钠的反应:3NO2+2OH-═NO3-+NO2-+2H2O | |
| D. | 向NaAlO2溶液中通入过量SO2:2AlO2-+SO2+3H2O═2A(OH)3↓+SO32- |
1.在Ca(OH)2(Ksp=5.5×10-6)、Mg(OH)2(Ksp=1.2×10-11)、AgCl(Ksp=1.56×10-10) 三种物质中,下列说法正确的是( )
| A. | Mg(OH)2不能转化为Ca(OH)2 | B. | Ca(OH)2的溶解度最小 | ||
| C. | Ca(OH)2不能转化为 Mg(OH)2 | D. | Ksp越大,S不一定越大 |
8.将某溶液逐滴加入Fe(OH)3胶体内,开始产生沉淀,继续滴加时沉淀又溶解,该溶液是( )
| A. | 2mol/L NaOH溶液 | B. | 2mol/LH2SO4溶液 | C. | 2mol/LMgSO4溶液 | D. | FeCl3溶液 |
18.下列说法正确的是( )
| A. | 容量瓶和分液漏斗使用前必须要检漏、干燥 | |
| B. | 可以用酒精萃取溶解在水中的碘 | |
| C. | 新制氯水应保存在棕色细口瓶中 | |
| D. | 某溶液焰色反应呈黄色,说明溶液中含有Na+,不含K+ |
5.下列有关有机物说法不正确的是( )
| A. | CH3CH(OH)CH2COOH系统命名法命名3-羟基丁酸 | |
| B. | 四苯基乙烯(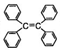 )中所有碳原子一定处于同一平面 )中所有碳原子一定处于同一平面 | |
| C. | lmol 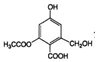 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol | |
| D. | 在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应 |
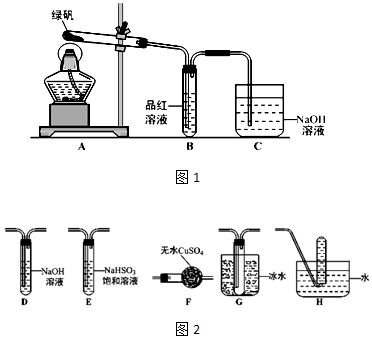
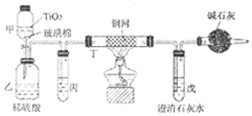
3.氰化物广泛应用于冶金、化工、医药等行业,因其对人畜及环境的巨大危害,需对含氰化物的废液进行深度处理.如处理含有NaCN的废液时,可在催化剂TiO2作用下,先用NaC1O将NaCN 氧化成NaCNO,再在酸性条件下继续被NaClO氧化,生成N2和CO2.环保工作人员在密闭系统中用如图装置进行实验,以证明处理方法的有效性.将含一定量NaCN的污水浓缩后与过量NaClO溶液混合倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.
(1)NaCN的电子式为Na+ .
.
(2)甲中反应的化学方程式为NaCN+NaClO=NaCNO+NaCl,乙中反应的离子方程式为2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O、2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O.
(3)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,丙中加入饱和食盐水,则装置的作用为除去氯气中的氯化氢.
(4)设计一个确定CN-被处理的百分率的实验方案过滤、洗涤、干燥、称量戊中沉淀的质量,计算出CN-被处理的百分率,装有碱石灰的干燥管的作用是防止空气中的二氧化碳进入戊装置影响沉淀测定的准确度.
(5)氢氰酸(HCN)是现代最早广泛使用的熏蒸之一,可以用于防治各种仓储害虫.在含有NaCN的废液中通入CO2可以制备氢氰酸.己知:
写出含NaCN的废液通入少量CO2发生反应的化学方程式NaCN+H2O+CO2=HCN+NaHCO3.

(1)NaCN的电子式为Na+
 .
.(2)甲中反应的化学方程式为NaCN+NaClO=NaCNO+NaCl,乙中反应的离子方程式为2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O、2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O.
(3)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,丙中加入饱和食盐水,则装置的作用为除去氯气中的氯化氢.
(4)设计一个确定CN-被处理的百分率的实验方案过滤、洗涤、干燥、称量戊中沉淀的质量,计算出CN-被处理的百分率,装有碱石灰的干燥管的作用是防止空气中的二氧化碳进入戊装置影响沉淀测定的准确度.
(5)氢氰酸(HCN)是现代最早广泛使用的熏蒸之一,可以用于防治各种仓储害虫.在含有NaCN的废液中通入CO2可以制备氢氰酸.己知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |