题目内容
物质的变化需要改变微粒之间的相互作用,所克服的作用属于同种类型的是
| A.Br2(l)和I2(s)分别受热气化 | B.NaBr和HI分别在水中电离 |
| C.硅和铁分别受热熔化 | D.氯化氢和蔗糖分别溶解于水 |
A
解析试题分析:A.Br2(l)和I2(s)分别受热气化克服的为分子间作用力,类型相同,故A正确; B.NaBr属于离子混合物,在水中电离需克服离子键,HI属于共价化合物,在水中电离需克服共价键,二者不同,故B错误;C.硅属于非金属单质,铁属于金属单质,熔化时分别克服共价键和金属键,故C错误;D.氯化氢在水中电离需克服共价键,蔗糖为非电解质,在水中不电离,溶于水克服分子间作用力,二者不同,故D错误.故选A.
考点:本题综合考查晶体的类型与粒子间的作用力,题目难度不大,注意晶体类型的判断以及粒子间作用力的异同.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
医学上在对抗癌物质的研究中发现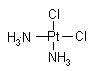 具有抗癌作用,而
具有抗癌作用,而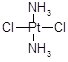 没抗癌作用。对此下列叙述正确的是( )
没抗癌作用。对此下列叙述正确的是( )
| A.两者互为同分异构体,都是以Pt原子为中心的四面体结构 |
| B.两者互为同分异构体,都是以Pt原子为中心的平面结构 |
| C.两者为同一物质,都是以Pt原子为中心的四面体结构 |
| D.两者为同一物质,都是以Pt原子为中心的平面结构 |
下列有关σ键和π键的说法正确的是
| A.σ键是镜像对称,而π键是轴对称 |
| B.π键是由两个p电子“头碰头”重叠形成的 |
| C.σ键可沿键轴自由旋转而不影响键的强度 |
| D.π键比σ键重叠程度大,形成的共价键强 |
下列关于化学变化的叙述错误的是
| A.化学变化一定伴随能量变化 |
| B.化学变化一定有化学键的断裂和生成 |
| C.化学变化一定伴随物质的状态变化 |
| D.化学变化一定有新物质生成 |
三氟化氮(NF3)在微电子工业中有重要用途,它在潮湿的空气中与水蒸气反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.NF3分子中含有非极性共价键 |
| B.NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下分解为CO和S。下列有关说法正确的是( )
| A.OCS、CO、CO2、S四种物质的晶体类型相同 |
| B.OCS高温分解时,碳元素化合价升高 |
| C.OCS分子中含有1个σ键和1个π键 |
| D.22.4 L OCS中约含有3×6.02×1023个原子 |
金星的大气中有一种称为硫化羰(COS)的分子,其结构与CO2类似,有关COS化学用语正确的是
A. | B.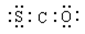 | C. | D.O="C=S" |
下面有关离子化合物的说法正确是
| A.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物。 |
| B.离子键只存在于离子化合物中,离子化合物中一定含有离子键 |
| C.离子化合物中不可能含有共价键 |
| D.离子化合物受热融化破坏化学键,吸收能量,属于化学变化 |