题目内容
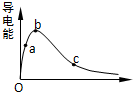 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,(1)O点导电能力为0的理由是
(2)a、b、c三点溶液的c(H+)由小到大的顺序是
(3)a、b、c三点醋酸的电离度最大的是
考点:电解质溶液的导电性,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)溶液是通过离子的定向移动形成电流的;
(2)溶液的导电能力与离子浓度成正比;
(3)溶液越稀,醋酸的电离程度越大.
(2)溶液的导电能力与离子浓度成正比;
(3)溶液越稀,醋酸的电离程度越大.
解答:
解:(1)溶液是通过离子的定向移动形成电流的,冰醋酸中醋酸以分子存在,不存在离子,所以冰醋酸不导电,故答案为:冰醋酸中不存在离子;
(2)溶液的导电能力与离子浓度成正比,根据图象知,溶液导电能力大小顺序是b>a>c,则氢离子浓度由小到大顺序是c<a<b,故答案为:c<a<b;
(3)溶液越稀,醋酸的电离程度越大,根据图象知,溶液体积大小顺序是c>b>a,所以醋酸电离程度最大的是c,故答案为:c.
(2)溶液的导电能力与离子浓度成正比,根据图象知,溶液导电能力大小顺序是b>a>c,则氢离子浓度由小到大顺序是c<a<b,故答案为:c<a<b;
(3)溶液越稀,醋酸的电离程度越大,根据图象知,溶液体积大小顺序是c>b>a,所以醋酸电离程度最大的是c,故答案为:c.
点评:本题考查了弱电解质的电离,明确溶液导电能力的影响因素、弱电解质电离程度与溶液浓度的关系是解本题关键,正确分析图象即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子化合物,请通过对CaC2制C2H2的反应进行思考,从中得到启示,判断下列产物正确的是( )
| A、ZnC2水解生成乙炔C2H2 |
| B、Al4C3水解生成丙炔C3H4 |
| C、Mg2C3水解生成丙烯C3H6 |
| D、Li2C2水解生成乙烯C2H4 |
下列叙述中正确的是( )
| A、标准状况下,1mol任何物质的体积都约为22.4L |
| B、1mol任何气体的体积都约为22.4L |
| C、标准状况下,1molO2和N2的混合气体的体积约为22.4L |
| D、某气体含有NA个原子,该物质在标准状况下的体积一定是22.4L |

 碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下:
碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下: