题目内容
20.一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g),达到平衡后测得A气体的浓度为1mol•L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.7mol•L-1,则下列叙述正确的是( )| A. | 平衡向正反应方向移动 | B. | x+y=z | ||
| C. | C的体积分数升高 | D. | B的转化率降低 |
分析 保持温度不变,将容器的体积扩大两倍,如平衡不移动,A的浓度为0.5mol/L,小于实际A的浓度变为0.7mol/L,说明平衡向生成A的方向移动,即向逆反应移动,据此结合选项解答.
解答 解:保持温度不变,将容器的体积扩大两倍,如平衡不移动,A的浓度为0.5mol/L,小于实际A的浓度变为0.7mol/L,说明平衡向生成A的方向移动,即向逆反应移动,
A、由上述分析可知,平衡向逆反应移动,故A错误;
B、增大体积,压强减小,平衡向逆反应移动,压强减小平衡向气体物质的量增大的方向移动,即x+y>z,故B错误;
C、平衡向逆反应移动,减小压强平衡向气体物质的量增大的方向移动,气体的物质的量增大,C物质的量减小,故C的体积分数下降,故C错误;
D、平衡向逆反应方向移动,B的转化率降低,故D正确;
故选D.
点评 本题考查化学平衡移动,难度中等,利用假设法判断平衡移动方向是解题关键.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
3.已知:Fe+Cu2+═Fe2++Cu和2Fe3++Cu═2Fe2++Cu2+,则下列判断不正确的是( )
| A. | Fe3+、Cu2+、Fe2+氧化性依次减弱 | |
| B. | 可发生反应:Fe+2Fe3+═3Fe2+ | |
| C. | Fe、Fe2+、Cu还原性依次减弱 | |
| D. | 将铁、铜混合粉末放入FeCl3溶液中,铁粉先溶解 |
11.下列情境中,对分离原理说法错误的是( )
| A. | 沙里淘金,利用了沙子和金子的密度不同 | |
| B. | 海水晒盐,利用了水和NaCl的沸点不同 | |
| C. | 酒糟酿酒,利用了粮食和酒精分子的颗粒大小不同 | |
| D. | 植物油能萃取蔬菜汁中的植物精华--维生素,利用了维生素在水和油中溶解度不同 |
8.下列能达到实验目的是( )
| A. | 在量筒中加入一体积的水,再加入浓硫酸配制稀硫酸 | |
| B. | 用澄清石灰水检验CO中含有的CO2 | |
| C. | 用玻璃棒搅拌漏斗中的液体以加快过滤速度 | |
| D. | 加入盐酸以除去硫酸钠中的少许碳酸钠杂质 |
15.写出以石墨作电极电解盐酸的电极反应式:
阳极:2Cl--2e-═Cl2↑
阴极:2H++2e-═H2↑
总反应:2HCl$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑.
阳极:2Cl--2e-═Cl2↑
阴极:2H++2e-═H2↑
总反应:2HCl$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑.
12.在标准状况下,相同质量的下列气体体积最小的是( )
| A. | O2 | B. | CO2 | C. | H2 | D. | SO2 |
10.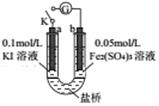 某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )
某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )
 某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )
某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )| A. | 指针第一次偏转时,b极反应式为Fe3++e-═Fe2+ | |
| B. | 加入AgNO3后,a为正极 | |
| C. | 当b极有0.001molFe3+被还原时,则通过盐桥的电子数为0.001NA | |
| D. | 第二次指针偏转的原因是:I-浓度减小,反应逆向进行 |
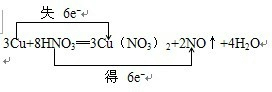 ,该反应中氧化剂是硝酸,氧化产物与还原产物的物质的量之比为3:2.
,该反应中氧化剂是硝酸,氧化产物与还原产物的物质的量之比为3:2.