题目内容
6.钛号称“崛起的第三金属”,因具有密度小、强度大、无磁性等优良的机械性能,被广泛应用于军事、医学等领域.已知钛有48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是( )| A. | 上述钛原子中,中子数不可能为22 | |
| B. | 钛元素在周期表中处于第四周期ⅡB族 | |
| C. | 钛原子的外围电子层排布为3d24s2 | |
| D. | 钛元素位于元素周期表的d区,是过渡元素 |
分析 A.质量数-质子数=中子数,钛的原子序数为22;
B.第三周期稀有气体的原子序数为18,根据钛的原子序数为22判断其在周期表中位置;
C.根据构造原理写出钛的基态电子排布式,然后判断其外围电子层排布;
D.Ti最后填充的电子为3d电子.
解答 解:A.质量数-质子数=中子数,则48Ti、49Ti、50Ti等中子数分别为26、27、28,故A正确;
B.第三周期稀有气体的原子序数为18,22-18=4,则钛在周期表中处于第四周期ⅣB族,故B错误;
C.钛的原子序数为22,其核外电子排布为:1s22s22p63s23p63d24s2,则钛原子的外围电子层排布为3d24s2,故C正确;
D.Ti最后填充的电子为3d电子,位于副族,则钛元素是d区的过渡元素,故D正确;
故选B.
点评 本题考查元素周期表的结构与应用,为高频考点,题目难度中等,明确同位素及原子的构成、电子排布与元素的位置为解答的关键,注重基础知识的考查.

练习册系列答案
相关题目
8.下列物质中的杂质(括号内为杂质)的检验、除杂试剂或方法正确的是( )
| 选项 | 物质及杂质 | 检验 | 除杂试剂或方法 |
| A | I2(Cl2) | 湿润的淀粉-KI试纸 | NaI溶液 |
| B | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
| C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和Na2CO3溶液 |
| D | NO(NO2) | 观察颜色或湿润的淀粉-KI试纸 | 水 |
| A. | A | B. | B | C. | C | D. | D |
17.下列说法正确的是( )
| A. | 热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据 | |
| B. | 升高温度或加入催化剂,不能改变化学反应的反应热 | |
| C. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| D. | 物质发生化学变化不一定伴随着能量变化 |
1.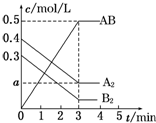 在一个容积为2L的密闭容器中,加入0.8mol A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)═2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.下列说法正确的是( )
在一个容积为2L的密闭容器中,加入0.8mol A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)═2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.下列说法正确的是( )
 在一个容积为2L的密闭容器中,加入0.8mol A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)═2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.下列说法正确的是( )
在一个容积为2L的密闭容器中,加入0.8mol A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)═2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示.下列说法正确的是( )| A. | 图中a点的值为0.05 | B. | 该反应的平衡常数K=0.03 | ||
| C. | 平衡时A2的转化率为62.5% | D. | 温度升高,平衡常数K值增大 |
15.下列关于反应热的叙述正确的是( )
| A. | 反应热就是反应发出的热量 | |
| B. | 由C(s)+$\frac{1}{2}$O2(g)═CO(g)的反应热为110.5kJ•mol-1,可知碳的燃烧热为110.5 kJ•mol-1 | |
| C. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | |
| D. | 1mol NaOH分别和1mol CH3COOH、1mol HNO3反应放出的热量:CH3COOH<HNO3 |
16.下列物质属于非电解质的是( )
| A. | NaOH | B. | Na2SO4 | C. | 酒精(C2H5OH) | D. | Cl2 |
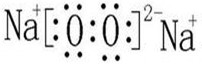 .
.