题目内容
已知反应2I-+S2O82-═I2+2SO42-,加入淀粉溶液可观察到溶液变蓝色.反应速率可以用淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.20℃时得到如下实验数据:
分析上述数据,下列说法正确的是( )
| 实验编号 | C(I-)/mol?L | C(S2O82-)/mol?L | t/s |
| 1 | 0.040 | 0.040 | 88.0 |
| 2 | 0.080 | 0.040 | 44.0 |
| 3 | 0.080 | 0.080 | 22.0 |
| 4 | 0.160 | 0.020 | 44.0 |
| 5 | 0.120 | 0.040 | 29.3 |
| A、该实验的目的是研究 I- 与S2O82- 的浓度对反应速率的影响 |
| B、I-的浓度越大,反应速率越快 |
| C、S2O82- 的浓度越小,反应速率越快 |
| D、5个实验中,编号3对应浓度的实验,反应速率最快 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:A.表中,I- 与S2O82- 的浓度不同,反应速率不通过;
B、C.反应速率取决于I- 与S2O82- 的浓度;
D.编号3对应浓度的实验用时最少,反应最快.
B、C.反应速率取决于I- 与S2O82- 的浓度;
D.编号3对应浓度的实验用时最少,反应最快.
解答:
解:A.由题目中表格数据可分析出c(I-)、c(S2O32-)浓度越大,反应速率越快,显蓝色所需时间越少,故实验目的应是研究反应物I-与S2O82-的浓度对反应速率的影响,故A正确;
B.反应速率取决于I- 与S2O82- 的浓度,如I-浓度较大,而S2O82- 浓度较小,则反应速率不一定大,故B错误;
C.如I-浓度不变,S2O82- 的浓度越小,反应速率越小,故C错误;
D.由表中数据可知,编号3对应浓度的实验用时最少,反应最快,故D正确.
故选AD.
B.反应速率取决于I- 与S2O82- 的浓度,如I-浓度较大,而S2O82- 浓度较小,则反应速率不一定大,故B错误;
C.如I-浓度不变,S2O82- 的浓度越小,反应速率越小,故C错误;
D.由表中数据可知,编号3对应浓度的实验用时最少,反应最快,故D正确.
故选AD.
点评:本题考查化学反应速、影响化学反应速率的外界因素(浓度)、学生对图表的观察、分析以及学生对实验数据的分析、整理、归纳等方面的思维能力,难度较大,解决该类试题应注意:①认真审题,明确实验目的,理解直接测量与实验目的间的逻辑和数学关系;②理解控制变量的思想在实验设计和数据分析中的运用.

练习册系列答案
相关题目
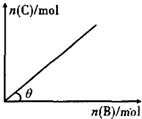 一定条件下,恒容的密闭容器中,加人一定量的A与B发生反应A(s)+2B(g)?C(g)+2D(g)△H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示.下列说法正确的是( )
一定条件下,恒容的密闭容器中,加人一定量的A与B发生反应A(s)+2B(g)?C(g)+2D(g)△H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示.下列说法正确的是( )| A、增加A的物质的量,正反应速率加快 |
| B、平衡时,其他条件不变,当温度升高时,θ变大 |
| C、图中曲线的斜率表示反应的化学平衡常数 |
| D、平衡时,其他条件不变,再通入B,则反应混合物的温度升高 |
下列说法不正确的是( )
| A、煤炭经气化,液化和干馏等过程,可获得清洁能源和重要的化工原料 |
| B、漂白粉和漂粉精不仅可以漂白棉,麻,纸张,还可做环境消毒剂 |
| C、Fe3O4俗称铁红,常做红色油漆和涂料 |
| D、蛋白质、淀粉、纤维素均属于天然有机高分子化合物 |
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A、氢氧燃料电池是一种具有应用前景的绿色电源 |
| B、该电池的总反应:2H2+O2=2H2O |
| C、外电路中电子由电极b通过导线流向电极a |
| D、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
下列化学反应对应的离子方程式正确的是( )
| A、Cl2与H2O的反应:Cl2+H2O=2H++Cl-+ClO- |
| B、FeCl3溶液与KI溶液跑反应:Fe3++2I-=Fe2++I2 |
| C、Cu与稀硝酸的反应:Cu+2H++NO3-=Cu2++NO↑+H2O |
| D、Al2O3与NaOH溶液的反应:Al2O3+2OH-+3H2O=2[Al(OH)4]- |
在常温下,纯水中存在电离平衡H2O?H++OH-,如要使水的电离程度增大,并使溶液的pH减小,应加入的物质是( )
| A、Al2(SO4)3 |
| B、NaHSO4 |
| C、Na2CO3 |
| D、HCl |
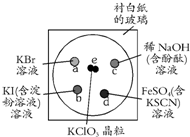 在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeSO4(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心处放置2粒芝麻大小的KClO3晶体,打开表面皿,向KClO3晶体滴加一滴浓盐酸,再立即将表面皿盖好,下列叙述不正确的是( )
在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeSO4(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心处放置2粒芝麻大小的KClO3晶体,打开表面皿,向KClO3晶体滴加一滴浓盐酸,再立即将表面皿盖好,下列叙述不正确的是( )| A、b处无色碘化钾溶液先变蓝色后变为无色,体现氯气和HClO的漂白性 |
| B、a处无色溴化钾溶液渐变成橙黄色,说明氯的非金属性强于溴 |
| C、c处氢氧化钠酚酞溶液的红色渐渐褪去,可能体现HCl的酸性或HClO的漂白性 |
| D、d处硫酸亚铁溶液呈红色,说明氯气氧化性强于Fe3+ |