题目内容
某研究性学习小组在网上搜集到信息:钾、钙、钠、镁等活泼金属能在CO2气体中燃烧.他们对钠在CO2气体中燃烧进行了下列实验:
(1)要熄灭燃烧的钠,可以选用的物质是 (填字母)
a.水 b.泡沫灭火剂 c.干沙土 d.二氧化碳
(2)该小组同学对瓶壁上的白色物质的成分进行讨论并提出假设
Ⅰ.白色物质是Na2O;
Ⅱ.白色物质是Na2CO3;
Ⅲ.白色物质还可能是
(3)为确定瓶壁上白色物质的成分,该小组进行了如下实验:
①通过对上述实验的分析,你认为上述三个假设中, 成立.
②钠在CO2中燃烧的化学方程式为 .
③丙同学认为白色物质有可能是氢氧化钠,你认为是否合理并说出理由 .
(4)某碳酸钠粉末中可能含有少量NaOH和NaCl杂质,为检验粉末中是否含有这些物质,某学生设计如下六个实验步骤,请将下面表格所用的试剂及实验操作补写完整:
| 操作过程 | 实验现象 |
| 将干燥的玻璃燃烧匙中燃烧的钠迅速伸入到盛有装满CO2的集气瓶中 | 钠在盛有CO2的集气瓶中继续燃烧 |
| 反应后冷却 | 集气瓶底附着黑色颗粒,瓶壁上附着有白色物质 |
a.水 b.泡沫灭火剂 c.干沙土 d.二氧化碳
(2)该小组同学对瓶壁上的白色物质的成分进行讨论并提出假设
Ⅰ.白色物质是Na2O;
Ⅱ.白色物质是Na2CO3;
Ⅲ.白色物质还可能是
(3)为确定瓶壁上白色物质的成分,该小组进行了如下实验:
| 实验步骤 | 实验现象 |
| ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
②钠在CO2中燃烧的化学方程式为
③丙同学认为白色物质有可能是氢氧化钠,你认为是否合理并说出理由
(4)某碳酸钠粉末中可能含有少量NaOH和NaCl杂质,为检验粉末中是否含有这些物质,某学生设计如下六个实验步骤,请将下面表格所用的试剂及实验操作补写完整:
| 实验步骤 | 所用试剂及实验操作 |
| ① | 取少量样品放入试管甲中,加入适量蒸馏水并振荡至全部溶解 |
| ② | |
| ③ | 过滤,将少量滤液盛在试管乙中 |
| ④ | 滴入几滴酚酞试液 |
| ⑤ | |
| ⑥ | 向溶液里滴入硝酸银溶液 |
考点:碱金属及其化合物的性质实验
专题:实验设计题
分析:(1)根据题干信息来分析,金属钠是一种活泼金属,用来灭火的物质和金属钠之间不能反应;
(2)白色固体还可能是氧化钠与碳酸钠的混合物;
(3)①氧化钠能与水反应生成氢氧化钠,氢氧化钠不能与氯化钙反应;
②依据方案①②的反应现象和结论,分析和推断钠在二氧化碳中燃烧生成碳酸钠和碳;
③依据反应物中的元素守恒分析判断生成物的组成元素;
(4)检验Na2CO3粉末中含有少量的NaOH和NaCl,取少量样品溶于水,滴加硝酸钡,过滤后,滴加酚酞可证明NaOH存在,然后再向滤液中滴加硝酸银生成白色沉淀,可证明含NaCl,以此来解答.
(2)白色固体还可能是氧化钠与碳酸钠的混合物;
(3)①氧化钠能与水反应生成氢氧化钠,氢氧化钠不能与氯化钙反应;
②依据方案①②的反应现象和结论,分析和推断钠在二氧化碳中燃烧生成碳酸钠和碳;
③依据反应物中的元素守恒分析判断生成物的组成元素;
(4)检验Na2CO3粉末中含有少量的NaOH和NaCl,取少量样品溶于水,滴加硝酸钡,过滤后,滴加酚酞可证明NaOH存在,然后再向滤液中滴加硝酸银生成白色沉淀,可证明含NaCl,以此来解答.
解答:
解:(1)a.钠和水能反应生成可燃性气体氢气,所以水不能灭火,故a错误;
b.泡沫灭火器产生二氧化碳气体,金属钠在二氧化碳中能燃烧,所以不能用泡沫灭火器灭火,故b错误;
c.干沙土能隔绝空气,所以细沙土能灭火,故c正确;
d.金属钠在二氧化碳中能燃烧,不能用二氧化碳灭火,故d错误;
故答案为:c;
(2)钠在二氧化碳中燃烧这一化学反应的反应物中只含有钠元素、碳元素和氧元素,没有氢元素,可能生成氧化钠或碳酸钠或二者的混合物,
故答案为:Na2O和Na2CO3的混合物;
(3)①氧化钠能与水反应生成氢氧化钠,氢氧化钠不能与氯化钙溶液反应产生白色沉淀,且其水溶液显碱性,碳酸钠能与氯化钙反应生成氯化钠和碳酸钙白色沉淀,故Ⅱ成立,故答案为:Ⅱ;
②依据现象和实验分析判断钠在二氧化碳气体中燃烧生成碳酸钠和碳单质,反应的化学方程式为:4Na+3CO2
2Na2CO3+C,故答案为:4Na+3CO2
2Na2CO3+C;
③丙同学认为白色物质有可能是氢氧化钠.是错误的,在反应过程中,是钠在二氧化碳气体中 的燃烧反应,无氢元素的存在,实验依据元素守恒可置换不可能生成氢氧化钠,
故答案为:不正确,因为反应物中无H元素(或违背质量守恒定律);
(4)检验Na2CO3粉末中含有少量的NaOH和NaCl,步骤为:①取少量样品,溶于水,②滴加过量硝酸钡溶液,③过滤后,④滴加酚酞可证明NaOH存在,⑤加入过量硝酸中和氢氧化钠溶液,⑥然后再向滤液中滴加过量硝酸银生成白色沉淀,
故答案为:加入过量硝酸钡溶液;加入过量的硝酸.
b.泡沫灭火器产生二氧化碳气体,金属钠在二氧化碳中能燃烧,所以不能用泡沫灭火器灭火,故b错误;
c.干沙土能隔绝空气,所以细沙土能灭火,故c正确;
d.金属钠在二氧化碳中能燃烧,不能用二氧化碳灭火,故d错误;
故答案为:c;
(2)钠在二氧化碳中燃烧这一化学反应的反应物中只含有钠元素、碳元素和氧元素,没有氢元素,可能生成氧化钠或碳酸钠或二者的混合物,
故答案为:Na2O和Na2CO3的混合物;
(3)①氧化钠能与水反应生成氢氧化钠,氢氧化钠不能与氯化钙溶液反应产生白色沉淀,且其水溶液显碱性,碳酸钠能与氯化钙反应生成氯化钠和碳酸钙白色沉淀,故Ⅱ成立,故答案为:Ⅱ;
②依据现象和实验分析判断钠在二氧化碳气体中燃烧生成碳酸钠和碳单质,反应的化学方程式为:4Na+3CO2
| ||
| ||
③丙同学认为白色物质有可能是氢氧化钠.是错误的,在反应过程中,是钠在二氧化碳气体中 的燃烧反应,无氢元素的存在,实验依据元素守恒可置换不可能生成氢氧化钠,
故答案为:不正确,因为反应物中无H元素(或违背质量守恒定律);
(4)检验Na2CO3粉末中含有少量的NaOH和NaCl,步骤为:①取少量样品,溶于水,②滴加过量硝酸钡溶液,③过滤后,④滴加酚酞可证明NaOH存在,⑤加入过量硝酸中和氢氧化钠溶液,⑥然后再向滤液中滴加过量硝酸银生成白色沉淀,
故答案为:加入过量硝酸钡溶液;加入过量的硝酸.
点评:本题考查物质的组成探究,为高频考点,题目难度中等,试题侧重于学生的分析能力和实验能力的考查,注重于物质性质的综合应用,根据反应现象正确判断反应产物是解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
铜有两种常见的氧化物CuO和Cu2O.某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示.则下列分析正确的是( )
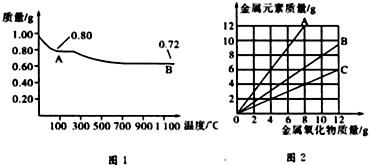

| A、图1中,A到B的过程中有0.01 mol电子发生了转移 |
| B、图1整个过程中共生成0.26 g水 |
| C、图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A |
| D、图1中A和B化学式分别为Cu2O和CuO |
下列金属中,不能从硫酸铜溶液里置换出铜的是( )
| A、Al | B、Zn | C、Fe | D、Na |
已知298K时,合成氨反应N2(g)+3H2(g)═2NH3(g)(可逆反应)△H=-92.2kJ?mol-1,此温度下,将1mol N2和3mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量(忽略能量损失) ( )
| A、一定大于92.2 kJ |
| B、一定小于92.2 kJ |
| C、一定等于92.2 kJ |
| D、无法确定 |
如图是某厂采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程.该方法对H2S的吸收率达99%以上,并可制取H2和S.下列说法正确的是( )

| A、可采取在足量空气中充分燃烧的方法消除H2S的污染 |
| B、反应②中的阴极反应式为2H++2e-═H2↑,电解后所得溶液呈酸性 |
| C、如反应①中H2S过量,则反应离子方程式为:2Fe3++3H2S═2FeS↓+S↓+6H+ |
| D、此反应流程图中可循环利用的物质是FeCl3溶液,FeCl3可用作杀菌、消毒剂和净水剂 |