题目内容
3.一种新型燃料电池,它是用两根金属做电极插入KOH溶液中,然后向两极上分别通甲烷和氧气,其电池反应为:X极:CH4+10OH--8e-=CO32-+7H2O
Y极:O2+4e-+2H2O=4OH-
下列关于此燃料电池的有关说法中错误的是( )
| A. | 通过甲烷的电极(X)为电池的负极,通过氧气的电极(Y)为电池正极 | |
| B. | 放电一段时间后,电解质溶液中KOH的物质的量不改变 | |
| C. | 在标准状况下,通过5.6L氧气,完全反应后有1.0mol的电子发生转移 | |
| D. | 放电时,通过甲烷的一极附近的pH降低 |
分析 甲烷碱性燃料电池工作时,正极发生还原反应,电极反应式为O2+4e-+2H2O=4OH-,甲烷在负极发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,结合电极方程式以及题目要求可解答该题.
解答 解:A.根据原电池总反应式可知甲烷被氧化,应为原电池的负极反应,氧气得电子被还原,应为原电池的正极反应,通甲烷的电极(X)为电池的负极,通氧气的电极(Y)为电池正极,故A正确;
B.根据总方程式CH4+2O2+2OH-═CO32-+2H2O可知反应消耗KOH,KOH的物质的量改变,故B错误;
C.n(O2)=$\frac{5.6L}{22.4L/mol}$=0.25mol,转移电子的物质的量为0.25mol×4=1mol,故C正确;
D.甲烷在负极发生氧化反应,通过甲烷电极的电极反应为CH4+10OH--8e-=CO32-+7H2O,所以负极附近的pH降低,故D正确.
故选B.
点评 本题考查了燃料电池知识,燃料电池电极反应式的书写要注意结合电解质溶液书写,原料相同,电解质溶液不同,电极反应式不同,如氢氧燃料电池,电解质为酸或碱时,电极反应式就不同,题目难度中等.

练习册系列答案
相关题目
18.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁均有水珠 | 两种物质均受热分解 |
| B | 向滴有酚酞的NaOH溶液中 通入SO2 | 溶液红色褪去 | SO2具有漂白性 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| A. | A | B. | B | C. | C | D. | D |
8. 环境问题已经是我国面临的重大问题.
环境问题已经是我国面临的重大问题.
Ⅰ.减少二氧化碳的排放是一项重要客题.研究表明,CO2经催化加氢可合成低碳醇.
CO2(g)+3H2(g)?CH3OH(g)+H20(g)△H
几种化学键的键能知表所示
(1)通过计算得出△H=-28kJ/mol.
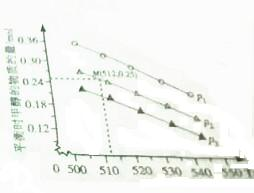
(2)在1.0L恒密闭容器中投入1molCO2和2.75molH2发生该反应,实验测得不同温度压强下,平衡时甲醇的物质的量如图所示.当压强为P2,温度为512K时,向该容器中投入1molCO2、0.5molH2、2molCH2OH、0.6molH2O,平衡向逆方向移动.
(3)以CH3OH、空气(O2含量20%)、KOH溶液为原料,以石墨为电极可直接构成燃料电池,则该电池的负极反应式为CH3OH+8OH--6e-=CO32-+6H2O,用该电池电解500mL1mol/LCuSO4溶液,当燃料电池消耗标况下56L空气时,计算理论上两极电解产生气体的总物质的量1mol.
 环境问题已经是我国面临的重大问题.
环境问题已经是我国面临的重大问题.Ⅰ.减少二氧化碳的排放是一项重要客题.研究表明,CO2经催化加氢可合成低碳醇.
CO2(g)+3H2(g)?CH3OH(g)+H20(g)△H
几种化学键的键能知表所示
| 化学键 | C=O | H-H | C-C | C-H | O-H | C-O |
| 键能/kJ、mol-1 | 803 | 436 | 332 | 409 | 463 | 326 |
(2)在1.0L恒密闭容器中投入1molCO2和2.75molH2发生该反应,实验测得不同温度压强下,平衡时甲醇的物质的量如图所示.当压强为P2,温度为512K时,向该容器中投入1molCO2、0.5molH2、2molCH2OH、0.6molH2O,平衡向逆方向移动.
(3)以CH3OH、空气(O2含量20%)、KOH溶液为原料,以石墨为电极可直接构成燃料电池,则该电池的负极反应式为CH3OH+8OH--6e-=CO32-+6H2O,用该电池电解500mL1mol/LCuSO4溶液,当燃料电池消耗标况下56L空气时,计算理论上两极电解产生气体的总物质的量1mol.
15.下列对有机物结构或性质的描述中错误的是( )
| A. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| B. | 乙烷和丙烯的物质的量共1mol,完成燃烧生成3molH2O | |
| C. | 1-丙醇和2-丙醇的一氯代物种类不同 | |
| D. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 |
12.铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )
①铊是易导电的银白色金属
②Tl(OH)3是两性氢氧化物
③Tl3+的氧化能力比Al3+强
④单质能和稀硝酸反应生成硝酸盐.
①铊是易导电的银白色金属
②Tl(OH)3是两性氢氧化物
③Tl3+的氧化能力比Al3+强
④单质能和稀硝酸反应生成硝酸盐.
| A. | ①④ | B. | ②③ | C. | ① | D. | ④ |
13.下列电极反应式正确的是( )
| A. | 以惰性材料为电极,KOH溶液为电解质构成原电池,负极反应式为H2-2e-=2H+ | |
| B. | 铜、锌在稀硫酸溶液中构成原电池,正极反应式为2H++2e-=H2↑ | |
| C. | 以铜为电极将2Fe3++Cu=2Fe2++Cu2+设计成原电池,正极反应式为Cu-2e-=Cu2+ | |
| D. | 以铝、铁为电极,在氢氧化钠溶液中构成原电池,负极反应式为Al-3e-=Al3+ |
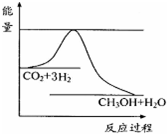 依据事实,写出下列反应的热化学方程式
依据事实,写出下列反应的热化学方程式