题目内容
9.在①乙醇与氧气在铜催化下反应;②淀粉在稀硫酸作用下在水中加热;③葡萄糖与钠反应;④乙醇一定条件下与乙酸反应中,不包括的反应类型是( )| A. | 氧化反应 | B. | 加成反应 | C. | 酯化反应 | D. | 水解反应 |
分析 乙醇含有羟基,可发生氧化、取代反应,淀粉在稀硫酸作用下发生水解反应,葡萄糖含有羟基,可由钠反应生成氢气,为取代反应,以此解答该题.
解答 解:①乙醇与氧气在铜催化下反应,为氧化反应,生成乙醛;
②淀粉在稀硫酸作用下在水中加热,为水解反应,也为取代反应;
③葡萄糖与钠反应生成氢气,为取代反应;
④乙醇一定条件下与乙酸反应中,为酯化反应,也为取代反应,
则没有涉及到的反应为加成反应,
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于化学反应类型的判断,注意把握官能团的变化,难度不大,注意相关基础知识的积累.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
19.制烧碱所用盐水需两次精制.第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水.
已知:过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如表:
完成下列填空:
(1)过程Ⅰ除去的离子是SO42-.
(2)检测Fe3+是否除尽的方法是取少量过程II后的滤液于试管中,滴加几滴KSCN溶液,若溶液不变红,说明Fe3+已除尽,反之没除尽.
(3)过程Ⅰ选用BaCl2而不选用CaCl2,请运用表中数据解释原因BaSO4的溶解度比CaSO4的小,可将SO42-沉淀更完.
(4)除去Mg2+的离子方程式是2Mg2++2CO32-+H2O═Mg2(OH)2CO3↓+CO2↑.
(5)检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+即可,原因是在BaCO3、CaCO3、Mg2(OH)2CO3中,BaCO3的溶解度最大,若Ba2+沉淀完全,则说明Mg2+和Ca2+也沉淀完全.
第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:
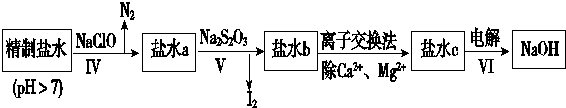
(6)过程Ⅳ除去的离子是NH4+、I-.
(7)过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释H+在阴极上得电子变成H2逸出,使H2O?H++OH-电离平衡向右移动,OH-在阴极区浓度增大,Na+向阴极区移动,最后NaOH在阴极区生成.
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水.
已知:过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如表:
完成下列填空:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
(2)检测Fe3+是否除尽的方法是取少量过程II后的滤液于试管中,滴加几滴KSCN溶液,若溶液不变红,说明Fe3+已除尽,反之没除尽.
(3)过程Ⅰ选用BaCl2而不选用CaCl2,请运用表中数据解释原因BaSO4的溶解度比CaSO4的小,可将SO42-沉淀更完.
(4)除去Mg2+的离子方程式是2Mg2++2CO32-+H2O═Mg2(OH)2CO3↓+CO2↑.
(5)检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+即可,原因是在BaCO3、CaCO3、Mg2(OH)2CO3中,BaCO3的溶解度最大,若Ba2+沉淀完全,则说明Mg2+和Ca2+也沉淀完全.
第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:

(6)过程Ⅳ除去的离子是NH4+、I-.
(7)过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释H+在阴极上得电子变成H2逸出,使H2O?H++OH-电离平衡向右移动,OH-在阴极区浓度增大,Na+向阴极区移动,最后NaOH在阴极区生成.
20.物质的量的单位是( )
| A. | 千克 | B. | 摩尔/升 | C. | 摩尔 | D. | 千米 |
17.区别下列各组中的两种物质的方法错误的是( )
| A. | 甲烷和乙烯:分别通入酸性KMnO4溶液 | |
| B. | 苯和四氯化碳:分别与水混合、振荡、静置 | |
| C. | 乙醇和乙酸:分别滴加NaOH溶液 | |
| D. | 棉花织品和羊毛织品:分别燃烧闻气味 |
4.下列有关性质比较不正确的是( )
| A. | 晶体熔点的高低: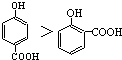 | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
1.下列说法正确的是( )
| A. | 可以用铝热反应制得单质镁 | |
| B. | 从海带中提取碘常用过氧化氢做还原剂 | |
| C. | 水华、赤潮等水体污染是由于含氮、磷的大量污水任意排放造成的 | |
| D. | 铝热剂就是指铝和氧化铁混合物 |