题目内容
15.下列实验装置图(有些图中部分夹持仪器未画出)能达到其实验目的是( )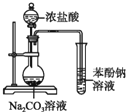 | 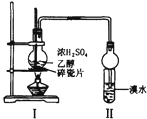 |
| A.证明酸性:盐酸>碳酸>苯酚 | B.溴水褪色一定产生了乙烯 |
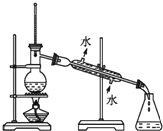 | 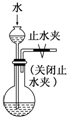 |
| C.分离溴乙烷和水 | D. 检查装置的气密性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.HCl也能和苯酚钠反应生成苯酚而影响碳酸和苯酚钠的反应;
B.浓硫酸被还原生成的二氧化硫能被溴氧化而使溴水褪色;
C.互不相溶的液体采用分液方法分离提纯;
D.能产生压强差的装置能检验装置气密性.
解答 解:A.浓盐酸具有挥发性,生成的二氧化碳中含有HCl,HCl也能和苯酚钠反应生成苯酚而影响碳酸和苯酚钠的反应,故A错误;
B.浓硫酸被还原生成的二氧化硫能被溴氧化而使溴水褪色,所以生成的气体应该先用NaOH溶液除去二氧化硫,然后用溴水检验,故B错误;
C.互不相溶的液体采用分液方法分离提纯,水和溴乙烷不互溶,可以采用分液方法分离提纯,故C错误;
D.关闭止水夹后,如果不漏气,不能形成压强差,所以水不漏下,故能检验装置的气密性,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及气密性检验、物质分离和提纯、物质检验等知识点,明确实验原理、物质性质差异性是解本题关键,注意AB中干扰的物质,为易错点.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
6.将铁、铝的混合物加入到足量氢氧化钠溶液中,充分反应后过滤,再将过滤得到的固体加入到足量的硫酸铜溶液中,充分反应后过滤得到的固体质量正好与原固体质量相等,则原固体中铝的质量分数为( )
| A. | 14.3% | B. | 12.5% | C. | 87.5% | D. | 85.7% |
3.现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是146C(用元素符号表示)元素Z的离子结构示意图为 .
.
(2)元素Y的与氢元素形成一种离子YH4+,则检验溶液中存在该离子的方法是取少许溶液(或待测液),加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在NH4+,反之,不存在NH4+.
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
(4)元素X与元素Y相比,非金属性较强的是N(用元素符号表示).下列表述中证明这一事实的是bc.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物水化物的酸性比X的最高价氧化物水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z三种元素的单质中化学性质明显不同于其他两种单质是Al(用元素符号表示),理由Al为金属单质,其余为非金属单质.
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
 .
.(2)元素Y的与氢元素形成一种离子YH4+,则检验溶液中存在该离子的方法是取少许溶液(或待测液),加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在NH4+,反之,不存在NH4+.
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
(4)元素X与元素Y相比,非金属性较强的是N(用元素符号表示).下列表述中证明这一事实的是bc.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物水化物的酸性比X的最高价氧化物水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z三种元素的单质中化学性质明显不同于其他两种单质是Al(用元素符号表示),理由Al为金属单质,其余为非金属单质.
10.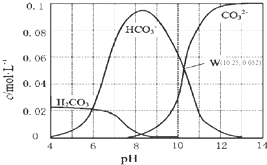 25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )
25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )
 25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )
25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )| A. | 在pH=7.0时,溶液中含碳粒子只有CO32-和HCO3- | |
| B. | 0.1 mol•L-1Na2CO3溶液pH=13 | |
| C. | H2CO3的Ka2=1.0×10-10.25 | |
| D. | 向100 mL 0.1 mol•L-1碳酸钠溶液中滴加盐酸至溶液pH=4.0,生成标准状况下CO2气体224 mL |
7.根据图中包含的信息分析,下列叙述正确的是( )
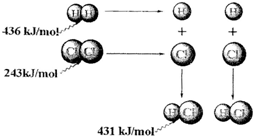

| A. | 氢气与氯气反应生成1 mol氯化氢气体,反应吸收248 kJ的能量 | |
| B. | 436 kJ/mol是指断开1 mol H2中的H-H键需要放出436 kJ的能量 | |
| C. | 431kJ/mol是指生成2 mol HCl中的H-Cl键需要放出431 kJ的能量 | |
| D. | 氢气与氯气反应生成2 mol氯化氢气体,反应放出183 kJ的能量 |
4.下列叙述中正确的是( )
| A. | 分子式相同,各元素的质量分数也相同的物质是同种物质 | |
| B. | 通式相同的不同物质一定是同分异构体 | |
| C. | 分子式相同的不同物质一定是同分异构体 | |
| D. | 相对分子质量相同的不同物质一定是同分异构体 |
5.如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).
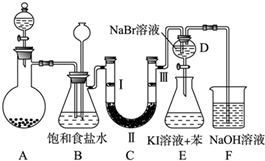
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置B中饱和食盐水的作用是除去Cl2中混有的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中有水柱上升.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d.
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为黄(橙黄、橙色、橙红等)色,打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
(5)如果将过量二氧化锰与20mL 12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气小于0.06mol.(填“大于”“小于”“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的质量为14.6g.

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置B中饱和食盐水的作用是除去Cl2中混有的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中有水柱上升.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d.
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
(5)如果将过量二氧化锰与20mL 12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气小于0.06mol.(填“大于”“小于”“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的质量为14.6g.