题目内容
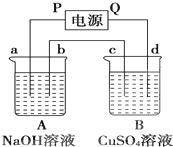 按如图装置实验,A、B两烧杯分别盛放200g10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出.又测得烧杯A溶液的质量减少4.5g,电极均为石墨电极,试回答:
按如图装置实验,A、B两烧杯分别盛放200g10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出.又测得烧杯A溶液的质量减少4.5g,电极均为石墨电极,试回答:(1)电源P端为
(2)b极产生气体的体积为
(3)c极上析出沉淀的质量为
(4)d极上所发生的电极反应式:
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)A、B为电解池,电解时,c电极上有Cu析出,则c为阴极,d为阳极,A、B为串联,所以a是阴极、b是阳极,P是负极、Q是正极;
(2)电解NaOH溶液时,实质上是电解水,A溶液的质量减少4.5g,即电解4.5g水,b为阳极,阳极上氢氧根离子放电生成氧气,根据原子守恒计算n(O2),再根据V=nVm计算气体体积;
(3)根据转移电子相等计算c电极析出金属质量;
(4)d电极是阳极,阳极上氢氧根离子放电生成氧气.
(2)电解NaOH溶液时,实质上是电解水,A溶液的质量减少4.5g,即电解4.5g水,b为阳极,阳极上氢氧根离子放电生成氧气,根据原子守恒计算n(O2),再根据V=nVm计算气体体积;
(3)根据转移电子相等计算c电极析出金属质量;
(4)d电极是阳极,阳极上氢氧根离子放电生成氧气.
解答:
解:(1)A、B为电解池,电解时,c电极上有Cu析出,则c为阴极,d为阳极,连接电源负极的电极为阴极、连接电源正极的电极是阳极,所以P是负极、Q是正极,故答案为:负;
(2)电解NaOH溶液时,实质上是电解水,A溶液的质量减少4.5g,即电解4.5g水,b为阳极,阳极上氢氧根离子放电生成氧气,n(H2O)=
=0.25mol,根据原子守恒得n(O2)=
×0.25mol=
mol,氧气体积V=nVm=
mol×22.4L/mol=2.8L,
故答案为:2.8;
(3)根据(2)知,析出氧气物质的量为0.125mol,根据4OH--4e-=2H2O+O2↑得转移电子的物质的量=0.125mol×4=0.5mol,串联电路中转移电子相等,所以析出Cu的质量=
×64g/mol=16g,故答案为:16;
(4)d电极是阳极,阳极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑.
(2)电解NaOH溶液时,实质上是电解水,A溶液的质量减少4.5g,即电解4.5g水,b为阳极,阳极上氢氧根离子放电生成氧气,n(H2O)=
| 4.5g |
| 18g/mol |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 8 |
故答案为:2.8;
(3)根据(2)知,析出氧气物质的量为0.125mol,根据4OH--4e-=2H2O+O2↑得转移电子的物质的量=0.125mol×4=0.5mol,串联电路中转移电子相等,所以析出Cu的质量=
| 0.5mol |
| 2 |
(4)d电极是阳极,阳极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑.
点评:本题考查电解原理,根据c电极判断阴阳极,从而确定正负极,会正确书写各个电极上发生的反应,知道离子放电顺序,注意串联电路中转移电子相等,题目难度不大.

练习册系列答案
相关题目
同温同压下,某容器充满O2重116g,若充满CO2重122g,现充满某气体重124g,则某气体的相对分子质量为( )
| A、24 | B、32 | C、40 | D、48 |
 如图装置,试管中盛有水,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )
如图装置,试管中盛有水,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )| A、U形管内红色退去 |
| B、试管内溶液变红 |
| C、气球a变瘪 |
| D、U形管水位d>c |
 某校化学兴趣小组的同学用如图装置进行实验,已知分液漏斗、小试管中均盛有水.请回答下列问题:
某校化学兴趣小组的同学用如图装置进行实验,已知分液漏斗、小试管中均盛有水.请回答下列问题: