题目内容
将表面被氧化Na2O、Na2O2的金属钠1.5g投入水中,收集到336mL气体(标准状况),该气体引爆后,冷却到原状态时,无气体剩余,分别求出Na、Na2O、Na2O2的质量.
考点:有关混合物反应的计算,化学方程式的有关计算
专题:计算题
分析:Na、Na2O、Na2O2 的混合物与足量的水反应得到的气体是氢气和氧气的混合物,将该混合气体通过放电,发生反应2H2+O2
2H2O,气体恰好完全反应,说明氢气和氧气反应的物质的量之比为2:1,根据生成标况下气体体积计算出氢气和氧气总的物质的量,根据方程式计算氢气、氧气的物质的量,进而再根据方程式计算Na、Na2O2的物质的量,根据m=nM计算出其质量,最后计算出计算Na2O的质量.
| ||
解答:
解:标准状况下336mL气体的物质的量为:
=0.015mol,
该气体为氢气和氧气的混合气体,该气体引爆后,冷却到原状态时,无气体剩余,气体恰好完全反应,根据反应2H2+O2═2H2O可知,混合气体中氢气的物质的量为:n(H2)=0.015mol×
=0.01mol,氧气的物质的量为:0.005mol,
氢气为钠与水反应生成的,根据反应2Na+2H2O=2NaOH+H2↑可知,金属钠的物质的量为:0.01mol×=0.02mol,其质量为:23g/mol×0.02mol=0.46g;
氧气为过氧化钠与水反应生成的,根据反应2Na2O2+2H2O=4NaOH+O2↑可知过氧化钠的物质的量为:0.005mol×2=0.01mol,过氧化钠的质量为:78g/mol×0.01mol=0.78g;
则混合物中氧化钠的质量为:1.5g-0.46g-0.78g=0.26g,
答:Na、Na2O、Na2O2的质量分别为:m(Na)=0.46g、m(Na2O2)=0.78g、m(Na2O)=0.26g.
| 0.336L |
| 22.4L/mol |
该气体为氢气和氧气的混合气体,该气体引爆后,冷却到原状态时,无气体剩余,气体恰好完全反应,根据反应2H2+O2═2H2O可知,混合气体中氢气的物质的量为:n(H2)=0.015mol×
| 2 |
| 1+2 |
氢气为钠与水反应生成的,根据反应2Na+2H2O=2NaOH+H2↑可知,金属钠的物质的量为:0.01mol×=0.02mol,其质量为:23g/mol×0.02mol=0.46g;
氧气为过氧化钠与水反应生成的,根据反应2Na2O2+2H2O=4NaOH+O2↑可知过氧化钠的物质的量为:0.005mol×2=0.01mol,过氧化钠的质量为:78g/mol×0.01mol=0.78g;
则混合物中氧化钠的质量为:1.5g-0.46g-0.78g=0.26g,
答:Na、Na2O、Na2O2的质量分别为:m(Na)=0.46g、m(Na2O2)=0.78g、m(Na2O)=0.26g.
点评:本题考查了混合物反应的计算,题目难度中等,明确反应原理为解答关键,注意掌握有关混合物反应计算的常用方法,试题培养了学生的化学计算能力.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
除去某溶液里溶解的少量杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A、FeCl2溶液(FeCl3):加过量还原铁粉,过滤 |
| B、KNO3溶液(AgNO3):加过量KCl 溶液,过滤 |
| C、NaCl溶液(I2):加CCl4,分液 |
| D、KNO3溶液(NaCl):加热蒸发得浓溶液后,降温、过滤 |
下列说法正确的是( )
| A、绿色食品是不含任何化学物质的食品 |
| B、Na2O2与CO2反应,Na2O2是氧化剂、CO2是还原剂 |
| C、与同浓度的硫酸反应时,NaHCO3比Na2CO3剧烈 |
| D、称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,则放出氢气的体积(同温同压下)不相等 |
纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体.下列区分这两种物质的方法正确的是( )
| A、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 |
| B、用洁净铁丝蘸取两种样品在煤气火焰上灼烧,火焰颜色呈黄色的是小苏打 |
| C、分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 |
| D、先将两样品配成溶液,后分别加入石灰水,无白色沉淀生成的是小苏打 |
化学与生活密切相关.下列说法不正确的是( )
| A、大力发展新能源是减少大气中SO2、NO2、可吸入颗粒物的措施之一 |
B、 在运输汽油的油罐车上所贴的化学危险标志如图 |
| C、为消除碘缺乏症,卫生部规定必须在食盐中加碘单质 |
| D、铜盐溶液都有毒,能使蛋白质变性 |

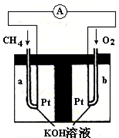 燃料电池(Fuel Cell)是一种将存在于燃料与氧化剂中的化学能直接转化为电能的发电装置.燃料和空气分别送进燃料电池,电就被奇妙地生产出来.它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电”而是一个“发电厂”.
燃料电池(Fuel Cell)是一种将存在于燃料与氧化剂中的化学能直接转化为电能的发电装置.燃料和空气分别送进燃料电池,电就被奇妙地生产出来.它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电”而是一个“发电厂”.